
| 选项 | 需要区分的物质 | 实验方法 | |
| A | 磷酸钙和氯化铵 | 溶于水 | 与熟石灰混合研磨 |
| B | 氢氧化钠固体和熟石灰 | 将两种固体溶于水 | 溶于水,向所得溶液中分别吹入CO2气体 |
| C | 硫酸钾和碳酸钾 | 加硝酸钡溶液 | 加水溶解 |
| D | 硬水和软水 | 肥皂水 | 加热、煮沸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.磷酸钙难溶,氯化铵易溶,铵态氮肥会与碱反应生成氨气;
B.氢氧化钠固体和熟石灰溶于水均放热,氢氧化钙与二氧化碳反应生成沉淀;
C.硫酸钾和碳酸钾与硝酸钡均能生成沉淀;
D..肥皂水在硬水和软水中的现象不同,硬水煮沸会出现白色沉淀.
解答 解:A.磷酸钙难溶,氯化铵易溶,现象不相同,能鉴别;加入熟石灰研磨,有刺激性气味的气体产生的是氯化铵,没有明显现象的是磷酸钙,现象不同,可以鉴别,故A正确;
B.氢氧化钠固体和熟石灰溶于水均放热,现象相同不能鉴别,氢氧化钠与二氧化碳反应无现象,氢氧化钙与二氧化碳反应生成沉淀,第一种方法不能鉴别,故B错误;
C.硫酸钾和碳酸钾与硝酸钡均能生成沉淀,两种现象相同不能鉴别,加水都能溶解,现象相同,故C错误;
D.取样品,加入肥皂水,中的,产生泡沫较多的是软水,产生泡沫较少的是硬水,现象不同,可以鉴别;加热、煮沸,有沉淀生成的是硬水,没有明显现象的是软水,现象不同,可以鉴别,故D正确.
故选:AD.
点评 本题考查了物质的鉴别,在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 在75℃左右,用HgSO4做催化剂,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种:现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图所示,请回答下列问题;
在75℃左右,用HgSO4做催化剂,乙炔可水化为乙醛,但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种:现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图所示,请回答下列问题;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaF 的水解产物是NaOH 和HF | B. | CaO2 的水解产物是Ca(OH)2 和H2O2 | ||
| C. | PCl3 的水解产物之一是PH3 | D. | Mg3N2水解产物是Mg(OH)2和NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(g)△H=-48.40 kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-5518 kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=+5518 kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-48.40 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
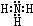 ,B的结构式为
,B的结构式为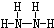 .
.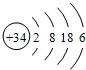 .
.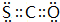 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸比磷酸易挥发 | |
| B. | 金刚石的熔点比晶体硅高 | |
| C. | 惰性气体一般很难发生化学反应 | |
| D. | 通常情况下单质溴呈液态、碘呈固态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com