
分析 (1)将反应②×2-①可得2N2H4+2NO2=3N2+4H2O,反应中只有N元素化合价发生变化,为NO2氧化剂,N2H4为还原剂;
(2)将②+③×2+④可得N2H4和H2O2反应生成液态水的热化学方程式,并结合③得到生成气态水的热化学方程式;
(3)将②-⑤×3+⑥×4可得联氨与氟气反应的热化学方程式.
解答 解:(1)将反应②×2-①可得2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1135.7KJ•mol-1,反应中只有N元素化合价发生变化,为NO2氧化剂,N2H4为还原剂,由方程式可知生成3molN2转移8mol电子,只有C错误,
故答案为:C;
(2)将②+③×2+④可得N2H4和H2O2反应生成液态水,反应的热化学方程式为N2H4(g)+2H2O2(1)=N2(g)+4H2O(l)△H=-818.4KJ•mol-1,
则生成气态水的热化学方程式为N2H4(g)+2H2O2(1)=N2(g)+4H2O(g)△H=-642.4KJ•mol-1,
生成1mol液态水放出热量为$\frac{818.4}{4}$kJ=204.6kJ,
故答案为:N2H4(g)+2H2O2(1)=N2(g)+4H2O(g)△H=-642.4KJ•mol-1;204.6;
(3)将②-⑤×3+⑥×4可得联氨与氟气反应的热化学方程式为2N2H4(g)+2F2(g)=N2(g)+4HF (g)△H=-1126kJ•mol-1,
故答案为:2N2H4(g)+2F2(g)=N2(g)+4HF (g)△H=-1126kJ•mol-1.
点评 本题考查较为综合,涉及化学反应与能量以及氧化还原反应知识,题目难度中等,注意把握盖斯定律的应用以及热化学方程式的书写.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚俗名石炭酸,向苯酚溶液中滴入石蕊试液溶液变浅红色 | |
| B. | 将金属钠放入乙醇中,反应较缓和且钠在液面下 | |
| C. | 既能够与酸反应又能够与碱反应的物质是两性化合物 | |
| D. | 淀粉、脂肪和纤维素都是天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
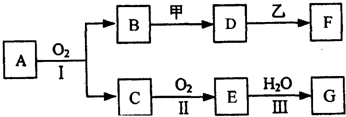
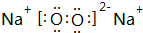 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极附近SO42- 逐渐增大 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 反应一段时间后,溶液的H+浓度降低 | |
| D. | 铜片上有H2逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙氨酸与苯丙氨酸脱水,最多可以生成3种二肽 | |
| B. | 对苯二甲酸(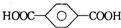 )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚酯纤维 )与乙二醇(HOCH2CH2OH)能通过加聚反应制取聚酯纤维( 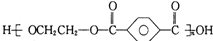 ) ) | |
| C. | 迷迭香酸的结构为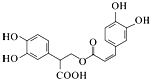 它可以发生酯化、水解、加成、取代、氧化等反应 它可以发生酯化、水解、加成、取代、氧化等反应 | |
| D. | 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在100℃时,将0.100mol 的四氧化二氮气体充入 1L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:
在100℃时,将0.100mol 的四氧化二氮气体充入 1L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)(mol/L) | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)(mol/L) | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com