
【题目】下表为某有机物与各种试剂的反应现象,则这种有机物可能是( )
试剂 | 钠 | 溴水 | NaHCO3 溶液 |
现象 | 放出气体 | 褪色 | 放出气体 |
A.CH2=CH—CH2—OHB.CH2=CH—COOH
C.![]() D.CH3COOH
D.CH3COOH
【答案】B
【解析】
有机物中能与Na反应放出气体的官能团是羟基和羧基,能使溴水褪色的官能团是碳碳双键、碳碳叁键、苯酚、醛基等,能与NaHCO3反应放出气体的官能团是-COOH,据此分析;
有机物中能与Na反应放出气体的官能团是羟基和羧基,能使溴水褪色的官能团是碳碳双键、碳碳叁键、苯酚、醛基等,能与NaHCO3反应放出气体的官能团是-COOH,
A. 不含羧基,不能与NaHCO3溶液反应放出气体,故A不符合题意;
B. 含有碳碳双键和羧基,符合上述分析,故B符合题意;
C. 不含羟基、羧基,该有机物不能与Na、NaHCO3反应,故C不符合题意;
D. 该有机物不能使溴水褪色,故D不符合题意;
答案:B。


科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是
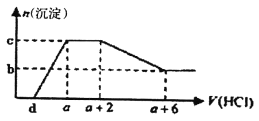
A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A. 3g 3He含有的中子数为1NA
B. 1 L 0.1 mol·L1磷酸钠溶液含有的![]() 数目为0.1NA
数目为0.1NA
C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA
D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的反应方程式不正确的是( )
A. 向碳酸钠溶液中滴加酚酞溶液,溶液变红:CO32-+2H2O![]() H2CO3+ 2OH-
H2CO3+ 2OH-
B. 以Na2S为沉淀剂,除去溶液中的Cu2+:Cu2+ + S2-===CuS↓
C. 向AgCl沉淀中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-![]() Ag2S+2Cl-
Ag2S+2Cl-
D. 向KI溶液中滴加稀硫酸和淀粉溶液,放置在空气中溶液变蓝:4H++4I-+O2=== 2I2 + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用氮化镓材料与铜组装如图所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。下列说法不正确的是

A. 该过程是将太阳能转化为化学能的过程
B. GaN表面发生氧化反应:2H2O-4 e-=== O2↑+4H+
C. Cu表面的反应是:CO2+8e-+6H2O === CH4+8OH
D. H+透过质子交换膜从左向右迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为1L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示,则下列表述中正确的是( )

A.该反应的化学方程式为2M![]() N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铬(Cr2O3)主要用于冶炼金属铬、有机化学合成的催化剂等.工业上是以铬铁矿[主要成份为Fe(CrO2)2,还含有Al2O3、SiO2等杂质]为主要原料进行生产,其主要工艺流程如下:

(1)亚铬酸亚铁[Fe(CrO2)2]中Cr的化合价是___________。
(2)焙烧时的主要反应为:4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2,其中被氧化的元素为___,每产生32g Fe2O3,转移电子的物质的量为_______,该步骤不能使用陶瓷容器,原因是_______。
8Na2CrO4+2Fe2O3+8CO2,其中被氧化的元素为___,每产生32g Fe2O3,转移电子的物质的量为_______,该步骤不能使用陶瓷容器,原因是_______。
(3)操作I包括过滤与洗涤,简述实验室中洗涤沉淀的操作:__________。
(4)硫磺在与铬酸钠的反应中转化为硫代硫酸钠,反应的离子方程式为___________,滤渣中除Al(OH)3外还有_______(填化学式)。
(5)某工厂用448 kg铬铁矿粉[含Fe(CrO2)280%]制备Cr2O3,最终得到产品182.4 kg,产率为______。
(6)Cr3+也有一定毒性,会污染水体,常温下要除去废液中多余的Cr3+,调节pH至少为_______,才能使铬离子沉淀完全 (已知:离子浓度小于1×10-5mol/L时沉淀就达完全, Cr(OH)3的Ksp=1.0×10-32)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA 为阿伏加德罗常数的值,下列说法不正确的是( )
A.0.l mol Cl2与足量的铁粉充分反应转移的电子数为 0.2 NA
B.1.0 mol CH4 与Cl2 在光照下反应生成的 CH3Cl 分子数为 1.0 NA
C.标准状况下,11.2 L甲烷和乙烯(C2H4)混合物中含氢原子数目为2 NA
D.0.1mol Cl2 通入水中,HClO、Cl-、ClO-粒子数之和小于 0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如右图所示。据图分析,下列判断错误的是

A. Ksp[Fe(OH)3]< Ksp [Cu(OH)2]
B. Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
C. 加适量NH4Cl固体可使溶液由a点变到b点
D. c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com