
 .
. 分析 (1)反应中高锰酸钾中的锰元素由+7价降为+2价,二氧化硫中的硫元素由+4价升高为+6价,依据氧化还原反应中得失电子守恒规律结合原子个数守恒规律配平书写方程式,依据方程式判断转移电子数与消耗二氧化硫关系;
(2)烷烃的通式为CnH2n+2,根据相对分子质量可知12n+2n+2=72,则n=5,该烷烃的分子式应为C5H12,跟氯气反应生成的一氯代物只有一种,说明结构对称,分子中只含有一种H,以此解答该题.
解答 解:(1)反应中高锰酸钾中的锰元素由+7价降为+2价,二氧化硫中的硫元素由+4价升高为+6价,要使得失电子守恒,则高锰酸钾系数为2,二氧化硫系数为5,依据原子个数守恒,方程式:5SO2 +2KMnO4+2H2O=K2SO4 +2MnSO4+2H2SO4,依据方程式每反应5mol二氧化硫,转移电子数为5mol×(6-4)=10mol电子,所以反应中转移5mole-,则消耗SO2物质的量为2.5mol;
故答案为:2;5;2;1;2;2;2.5mol;
(2)烷烃的通式CnH2n+2,该烷烃的相对分子质量为72,
所以有:12n+2n+2=72,即14n=70,
解得n=5,即分子式为C5H12.
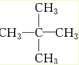
含5个碳原子的烷烃的一氯取代物只有一种,说明烃分子中12个氢原子的位置均是等效的,分子结构对称,
结构简式应为 ;
;
故答案为: .
.
点评 本题考查了氧化还原反应、有机物结简式的确定,明确氧化还原反应得失电子守恒规律、电子转移数目的计算方法、明确烷烃结构特点是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).
有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol/(L•min) | |
| B. | 6~10 min的平均反应速率:v(H2O2)<3.3×10-2 mol/(L•min) | |
| C. | 反应到6 min时,H2O2分解了50% | |
| D. | 反应到6 min时,c(H2O2)=0.30 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用点燃的方法鉴别甲烷,乙烯,丙烯和苯乙烯 | |
| B. | 1体积某气态烃完全燃烧生成的CO2比水蒸气少1体积(在相同条件下测定)可推知该烃为烷烃 | |
| C. | 等质量的乙醛和乙炔的耗氧量相同 | |
| D. | 任意比例混合的乙烯和1,3-丁二烯燃烧时只要总质量一定则生成的产物的质量也为定值 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加C的量 | |
| B. | 将容器的体积减小一半 | |
| C. | 保持体积不变,充入氮气使体系的压强增大 | |
| D. | 保持压强不变,充入氮气使体系的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的原子序数A>B>C | B. | 它们的离子半径A2->C->B2+ | ||
| C. | 它们的原子半径C>B>A | D. | 它们的最外层电子数C>A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com