
| A、180mL | B、120mL |
| C、90mL | D、60mL |
| 3.36L |
| 22.4L/mol |
| 0.6mol |
| 5mol/L |


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
| A、在水溶液中有H+电离的化合物一定属于酸 |
| B、CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
| C、Na2O、Na2O2均属于碱性氧化物 |
| D、有发光、发热、变色、生成气体或沉淀、爆炸等现象的不一定是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
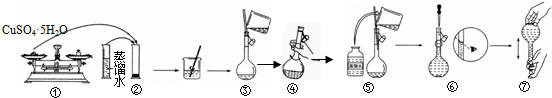
查看答案和解析>>
科目:高中化学 来源: 题型:
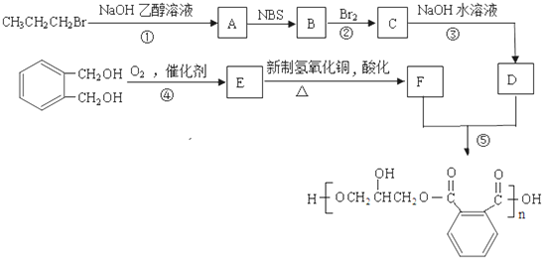
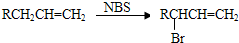
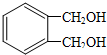 中的含氧官能团的名称为
中的含氧官能团的名称为 互为同分异构体的结构简式.
互为同分异构体的结构简式.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、196kJ |
| B、98kJ |
| C、<196kJ |
| D、>196kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度,溶液的pH增大 |
| B、c(Na+)+c(H+)=c(OH-)+C(HCO3-)+C(CO32-) |
| C、c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D、稀释溶液,溶液中所有离子的浓度都减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定 次数 | 待测溶液 的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com