
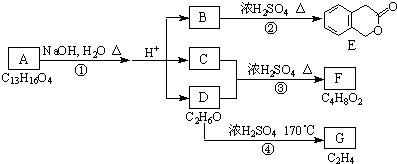
 .反应①的反应类型是水解反应.
.反应①的反应类型是水解反应. .
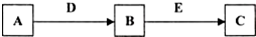
. 分析 B在浓硫酸加热条件下生成E,由E的结构可知,B发生酯化反应生成E,故B为 .D的分子式为C2H6O,一定条件下可以生成C2H4,故D为CH3CH2OH,G为CH2=CH2.C与CH3CH2OH在浓硫酸、加热条件下生成F,结合F的分子式C4H8O2可知,生成F的反应为酯化反应,故C为CH3COOH,F为CH3COOCH2CH3,A在氢氧化钠水溶液、加热条件下发生水解反应,酸化得到B、C、D,故A为
.D的分子式为C2H6O,一定条件下可以生成C2H4,故D为CH3CH2OH,G为CH2=CH2.C与CH3CH2OH在浓硫酸、加热条件下生成F,结合F的分子式C4H8O2可知,生成F的反应为酯化反应,故C为CH3COOH,F为CH3COOCH2CH3,A在氢氧化钠水溶液、加热条件下发生水解反应,酸化得到B、C、D,故A为
解答 解:B在浓硫酸加热条件下生成E,由E的结构可知,B发生酯化反应生成E,故B为 .D的分子式为C2H6O,一定条件下可以生成C2H4,故D为CH3CH2OH,G为CH2=CH2.C与CH3CH2OH在浓硫酸、加热条件下生成F,结合F的分子式C4H8O2可知,生成F的反应为酯化反应,故C为CH3COOH,F为CH3COOCH2CH3,A在氢氧化钠水溶液、加热条件下发生水解反应,酸化得到B、C、D,故A为
.D的分子式为C2H6O,一定条件下可以生成C2H4,故D为CH3CH2OH,G为CH2=CH2.C与CH3CH2OH在浓硫酸、加热条件下生成F,结合F的分子式C4H8O2可知,生成F的反应为酯化反应,故C为CH3COOH,F为CH3COOCH2CH3,A在氢氧化钠水溶液、加热条件下发生水解反应,酸化得到B、C、D,故A为
(1)由上述分析可知,D为CH3CH2OH,化学名称为乙醇,故答案为:乙醇;
(2)反应③是CH3COOH与CH3CH2OH发生酯化反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
(3)由上述分析可知,B为 ,分子式为C9H10O3,A的结构简式是
,分子式为C9H10O3,A的结构简式是
故答案为:C9H10O3;
(4)反应④是乙醇发生消去反应生成乙烯,反应方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
乙烯形成的高聚物为 ,反应方程式为:n CH2=CH2$\stackrel{催化剂}{→}$
,反应方程式为:n CH2=CH2$\stackrel{催化剂}{→}$ ,
,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;n CH2=CH2$\stackrel{催化剂}{→}$ .
.
点评 本题考查有机物的推断,注意根据转化关系中E的结构以及D、G的分子式进行推断,掌握官能团的性质与转化是关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 甲烷的电了式: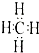 | B. | 乙炔的结构简式:CHCH | ||
| C. | 硫离子的结构示意图: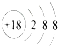 | D. | 中子数为10的原子:${\;}_{8}^{10}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
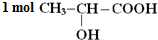 分别与Na、NaOH、NaHCO3完全反应时,消耗的Na、NaOH、NaHCO3的物质的量之比为2:1:1,写出该有机物和NaOH反应的化学方程式CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O.
分别与Na、NaOH、NaHCO3完全反应时,消耗的Na、NaOH、NaHCO3的物质的量之比为2:1:1,写出该有机物和NaOH反应的化学方程式CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液吸收过量的二氧化碳:OH-+CO2═HCO3- | |
| B. | 亚硫酸氢铵溶液与足量氢氧化钠溶液反应:HSO3-+OH-═SO32-+H2O | |
| C. | 氯气通入冷水中:Cl2+H2O═Cl-+ClO-+2H+ | |
| D. | 碳酸镁悬浊液中加醋酸:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
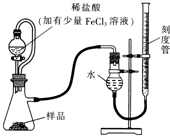 过氧化镁(MgO2)易溶于稀酸,溶于酸后会产生过氧化氢,在医学上可作为“解酸剂”等.过氧化镁产品中常会混有一定量的MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后会产生过氧化氢,在医学上可作为“解酸剂”等.过氧化镁产品中常会混有一定量的MgO,实验室可通过多种方案测定样品中过氧化镁的含量.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ②③ | C. | ②④ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
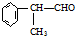 的物质,该物质是一种香料.
的物质,该物质是一种香料.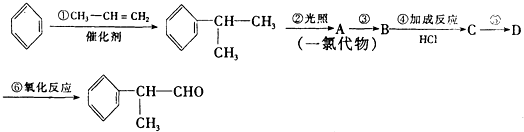
 .
. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2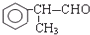 +2H2O.
+2H2O.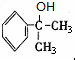 生成
生成 、
、 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com