
两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是
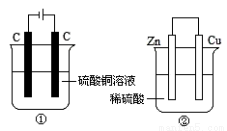
A.产生气体体积 ①=②
B.①中阴极质量增加,②中正极质量减小
C.电极反应式:①中阳极:4OH- - 4e- →2H2O+O2↑ ②中负极:2H++2e-→H2↑
D.溶液的pH变化:①减小,②增大
D
【解析】
试题分析:A、①是电解硫酸铜的反应,得到的气体是氧气,通过0.02mol电子时,产生0.005mol氧气;②是原电池装置,Zn与稀硫酸反应产生氢气,通过0.02mol电子时产生0.01mol氢气,二者的体积不同,错误;B、①中阴极析出Cu,所以阴极质量增加,②中正极是Cu,氢离子在Cu极放电产生氢气,但Cu极质量不变,错误;C、电极反应式:①中阳极发生氧化反应:4OH- - 4e- =2H2O+O2↑ ②中Zn是负极,发生氧化反应,所以负极:Zn-2e-=Zn2+,错误;D、①中氢氧根离子放电,导致溶液中氢离子浓度增大,所以溶液的pH减小;②中氢离子放电生成氢气,氢离子浓度减小,所以溶液的pH增大,正确,答案选D。
考点:考查电化学反应原理的应用,电极反应式的判断,溶液pH的变化


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:填空题
N是重要的非金属元素,尿素、羟胺、硝酸、亚硝酸钠均为重要的含氮化合物。
(1)尿素[CO(NH2)2]是人类利用无机物合成的第一种有机物。尿素中元素原子半径最大的原子结构示意图为 ;
(2)羟胺(NH2OH)可看做是氨分子内的1个氢原子被羟基取代的物质,常用作还原剂。
①利用羟胺的还原性,可以除去含Fe2+中的Fe3+,氧化产物是一种性质稳定、无污染的气体,写出反应的离子方程式
②制备NH2OH·HCl(盐酸羟胺)的一种工艺流程如下图所示:

ⅰ步骤中,发生反应的化学方程式为 ;
ⅱ步骤中使用的NaNO2外观酷似食盐,误食会中毒。可用电解法将工业废水中少量的NO2ˉ转化为N2以降低其危害。写出NO2ˉ在酸性条件下转化为氮气的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:选择题
只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称氢化物。下列物质不属于氢化物的是
A.H2O B.NaH C.H2SO4 D.NH3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省保定市高三12月联考化学试卷(解析版) 题型:选择题
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是

A.b极发生氧化反应
B.a极的反应式:N2H4+4OH--4e-=N2↑+4H2O
C.放电时,电流从a极经过负载流向b极
D.其中的离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省保定市高三12月联考化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中,能大量共存的是
A.含有NaClO的溶液中:K+,NH4+, Fe3+,Br-,SO32-
B.所含溶质为Na2S2O3的溶液:K+、SO42-、NO3-、H+
C.加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
D.使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省保定市高三12月联考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.常温常压下,44 g C3H8中含有的碳碳单键数为3 NA
C.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数为3 NA
D.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三11月月考化学试卷(解析版) 题型:实验题
(19分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
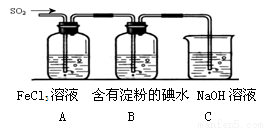
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释,这样操作的目的是 。
(2)装置C的作用是 。
(3)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、 、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
A.蒸发皿
B.石棉网
C.漏斗
D.烧杯
E.玻璃棒
F.坩埚
(4)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式 ;
②请设计实验方案检验有Fe2+生成 ;
③该小组同学向C烧杯反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42—。该做法 (填“合理”或“不合理”),理由是 。
(5)能表明I-的还原性弱于SO2的现象是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
水的状态除了气、液、固之外,还有玻璃态。它是由液态水急速冷却到165K时形成的,玻璃态的水无固态形状,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.玻璃态水是一种特殊的分子晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com