
| A. | 给定条件下,Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg,物质间转化能一步实现 | |
| B. | 工业上,常用电解熔融AlCl3的方法冶炼金属铝 | |
| C. | 火法炼铜:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,其中Cu2S既作氧化剂又作还原剂 | |
| D. | 铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,反应物刚好完全反应,反应后固体质量增加 |
分析 A.电解氯化镁溶液,氯离子在阳极失电子生成氯气,氢离子在阴极得到电子生成氢气,溶液中形成氢氧化镁沉淀;
B.氯化铝是共价化合物不能电离出离子;
C.Cu2S中铜元素化合价+1价变化为0价,硫元素化合价-2价变化为+4价,元素化合价升高做还原剂,元素化合价降低做氧化剂;
D.反应前后都是固体,固体质量不变.
解答 解:A.电解氯化镁溶液,氯离子在阳极失电子生成氯气,氢离子在阴极得到电子生成氢气,溶液中形成氢氧化镁沉淀,应是电解熔融氯化镁生成金属镁,故A错误;
B.氯化铝是共价化合物不能电离出离子,不能电解氯化铝制备铝,应是电解熔融氧化铝制备铝,故B错误;
C.火法炼铜:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,铜元素化合价+1价变化为0价,硫元素化合价-2价变化为+4价,其中Cu2S既作氧化剂又作还原剂,故C正确;
D.铝热法炼铁:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,反应物刚好完全反应,反应前后都是固体,固体质量不变,故D错误;
故选C.
点评 本题考查了金属制备原理的分析判断、氧化还原反应概念的分析、注意氯化铝是共价化合物不能电离,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,在0.10mol•L-1CH3COOH溶液中加入少量CH3COONa晶体,能使CH3COOH的电离度降低,溶液的pH增大 | |
| B. | 常温下向氯化铵溶液中加入少量氨水使溶液中c(NH4+)=c(Cl-),则混合液的pH=7 | |
| C. | pH均为5 的盐酸和硫酸氢钠溶液中,水的电离程度后者大 | |
| D. | pH=3的0.1 mol•L-1HA溶液与0.05 mol•L-1NaOH溶液等体积混合后所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
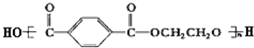
| A. | 合成涤纶纤维的单体为HOCH2CH2OH和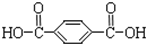 | |
| B. | 棉花和涤纶纤维在一定条件下均能水解 | |
| C. | 涤纶纤维和棉花均为混合物 | |
| D. | 棉花和涤纶纤维不能用燃烧法区别 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题



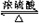 CH3COOCH2CH3+H2O;反应类型:酯化反应.
CH3COOCH2CH3+H2O;反应类型:酯化反应. ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | NH4NO3晶体中含共价键,是共价化合物 | |
| C. | H2O2、N2H4分子中只含有极性共价键 | |
| D. | 某化合物熔融状态能导电,可以证明该化合物内一定存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂 | 主要操作 |
| A | 乙炔 | H2S、PH3 | NaOH溶液 | 洗气 |
| B | 乙醛 | 乙酸 | Na2CO3溶液 | 分液 |
| C | 溴乙烷 | 溴单质 | NaHSO3溶液 | 分液 |
| D | CH3CH2OH | H2O | 熟石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4是一种酸 | |
| B. | NaHSO4溶液与Cu(OH)2反应的离子方程式:Cu(OH)2+2H+=Cu2++2H2O | |
| C. | NaHSO4溶液可使石蕊试液变蓝 | |
| D. | NaHSO4溶液与MgCl2溶液,BaCl2溶液反应均可生成白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
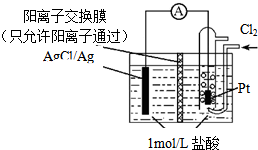
| A. | 正极反应为Ag-e-=Ag+ | |
| B. | 放电时,交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 用KCl溶液代替盐酸,则电池总反应不改变 | |
| D. | 当电路中转移0.1mol e-时,通过交换膜的阳离子为0.2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com