
| A. | 最终得到沉淀的质量大于$\frac{37m}{28}$g | |
| B. | 该饱和溶液质量百分比浓度为$\frac{s}{100+s}$% | |
| C. | 最终所得溶液c(OH-)不变 | |
| D. | 该饱和溶液中溶质物质的量浓度为$\frac{1000ρs}{74(100+s)}$mol/L |
分析 A.mg CaO溶于水发生反应:CaO+H2O═Ca(OH)2,反应生成氢氧化钙的质量为$\frac{37m}{28}$g,由于原饱和溶液中溶剂减少,则会析出部分溶质,所以得到沉淀的质量大于$\frac{37m}{28}$g;
B.饱和溶液中溶质质量分数w=$\frac{{m}_{溶质}}{{m}_{溶液}}$×100%=$\frac{溶解度}{100+溶解度}$×100%;
C.温度不变,饱和溶液中溶质的浓度不变,则溶液中氢氧根离子浓度不变;
D.根据c=$\frac{1000ρw}{M}$计算出该饱和溶液的物质的量浓度.
解答 解:A.mg CaO溶于水发生反应:CaO+H2O═Ca(OH)2,反应生成氢氧化钙的质量为:$\frac{74}{56}$×mg=$\frac{37m}{28}$g,由于原饱和溶液中溶剂减少,则会析出部分溶质,所以最终得到的沉淀的质量大于$\frac{37m}{28}$g,故A正确;
B.该饱和溶液的溶解度为sg,则该饱和溶液中溶质的质量分数为:$\frac{Sg}{100+sg}$×100%=$\frac{100s}{100+s}$%,故B错误;
C.最终得到的还是氢氧化钙的饱和溶液,由于温度相同,则溶液中氢氧根离子浓度不变,故C正确;
D.该饱和溶液的质量分数为:$\frac{Sg}{100+sg}$×100%,该溶液的物质的量浓度为:c=$\frac{1000ρw}{M}$=$\frac{1000ρs}{74(100+s)}$mol/L,故D正确;
故选B.
点评 本题考查了物质的量浓度与溶质质量分数的计算、饱和溶液的计算,题目难度中等,注意明确饱和溶液特点,熟练掌握物质的量浓度与溶质质量分数的转化关系.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe不能与水蒸气发生化学反应 | |
| B. | 白色Fe(OH)2在空气中放置最终变成灰绿色 | |
| C. | 铝可以与氢氧化钠溶液发生反应:2Al+2NaOH+2H2O═2NaAlO2+3H2↑ | |
| D. | 氯化铁溶液不能与铜单质发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
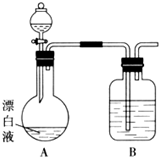 实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.
实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
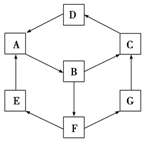 如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.
如图是无机物A~G在一定条件下的转化关系(部分产物及反应条件未列出).已知:①A、B、C、D、G含有同种元素.| 物质 | 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
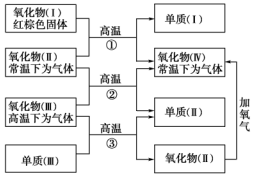 以下一些氧化物和单质之间可发生如图所示的反应:
以下一些氧化物和单质之间可发生如图所示的反应:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
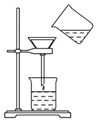 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
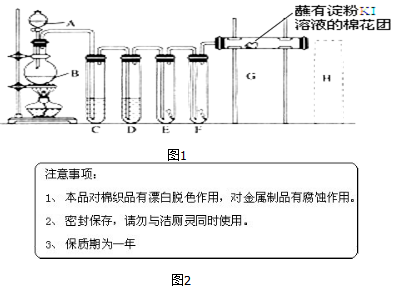
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
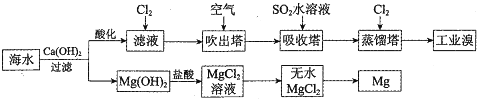
 _.通入氯气后,反应的离子方程式是Cl2+2Br-=Br2+2Cl-.海水调节pH过程可以看做发生盐酸和氢氧化钠的中和反应,常温下该反应的平衡常数在c(H2O)看做常数不列入表达式的情况下,数值是1014.调海水pH可提高Cl2的利用率,用平衡移动原理解释其原因是Cl2+H2O=H++Cl-+HClO,增大c(H+),平衡逆向移动,抑制Cl2与水的反应
_.通入氯气后,反应的离子方程式是Cl2+2Br-=Br2+2Cl-.海水调节pH过程可以看做发生盐酸和氢氧化钠的中和反应,常温下该反应的平衡常数在c(H2O)看做常数不列入表达式的情况下,数值是1014.调海水pH可提高Cl2的利用率,用平衡移动原理解释其原因是Cl2+H2O=H++Cl-+HClO,增大c(H+),平衡逆向移动,抑制Cl2与水的反应查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com