
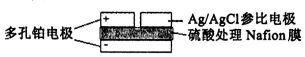
 ��������������������������Ҫ��Ӧ�ã�
��������������������������Ҫ��Ӧ�ã� S+2CO2��
S+2CO2������ ��1�����������ܹ�����ɫ���ʻ���������ɫ���ʣ�����Ư���ԣ�
��2��SO2���л�ԭ�ԣ��������������ʷ�Ӧ��
��3��SO2��CO��Ӧ���ɵ�������Ԫ�صĻ��ϼ۽��ͣ���̼Ԫ�صĻ��ϼ����ߣ��������ɶ�����̼��
��4�������������ɵķ�Ӧ���ڻ�ѧ�仯����̬���ʵõ�����ת��Ϊ����̬��
��5��SO2�õ���������S2O42-��
��� �⣺��1�����������ܹ�����ɫ���ʻ���������ɫ���ʣ�����Ư���ԣ����Գ�������ֽ��ӡȾ���õ���ɫ����
�ʴ�Ϊ��Ư�ף�
��2��SO2��SԪ��Ϊ+4�ۣ�SO2���л�ԭ�ԣ��������������ʷ�Ӧ������������ø�Ļ��ԣ�
�ʴ�Ϊ����ԭ�����ƣ�
��3��SO2��CO��Ӧ���ɵ�������Ԫ�صĻ��ϼ۽��ͣ���̼Ԫ�صĻ��ϼ����ߣ��������ɶ�����̼����Ӧ�ķ���ʽΪ��SO2+2CO  S+2CO2��
S+2CO2��
�ʴ�Ϊ��SO2+2CO  S+2CO2��
S+2CO2��
��4��SO2+h��1������⣩��SO2+��SO2+��S02ʮh��2 ��ӫ�⣩���ù�����û���������������������仯��SO2+h��1������⣩��SO2+��SO2����������������SO2+Ϊ����̬��
�ʴ�Ϊ��������������
��5��SO2�õ���������S2O42-���������ĵ缫����ʽΪ��2SO2+2e-=S2O42-��
�ʴ�Ϊ��2SO2+2e-=S2O42-��
���� ���⿼���˶�����������ʡ���ѧ����ʽ����д����ѧ�仯�������仯�����ԭ����Ӧ�ã���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͶԻ���֪ʶ��Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ǧ��о��ԭ����Ǧ����ͯ����ҧǦ�ʻᵼ��Ǧ�ж� | |
| B�� | ������ú¯�ľ������һ��ˮ�����Է�ֹCO�ж� | |
| C�� | ��ũ�������Ҵ�����ȼ��ú��������CO2������ֲ������� | |
| D�� | �ߴ���Ӧ���ڰ뵼��Ԫ���뼯��оƬ֮�У�����˵��������Ϣ���������Ĵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ����ʶ������ӻ����������ʶ��ǹ��ۻ����� | |
| B�� | ǿ����ʵ�ˮ��Һ�������ʷ��ӣ�������ʵ�ˮ��Һ�������ʷ��� | |
| C�� | ��FeBr2��Һ�м����������ˮ������������FeCl3���� | |
| D�� | ��Na2CO3������Һ�У�ͨ�������CO2�������ɵ�NaHCO3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol FeCl3���γɵĽ���������Ϊ0.1NA | |
| B�� | ������1L pH=12��ˮ�к���OH-��ĿΪ0.01NA | |
| C�� | 0.1mol02��ȫ��Ӧʱ��ת�Ƶĵ�����Ϊ0.4NA | |
| D�� | 12��̼�����������Ĺ��ۼ���Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
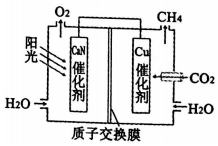
| A�� | ��װ����ԭ��� | |
| B�� | GaN�������淢��������Ӧ����Һ������ǿ | |
| C�� | ���Ӵ�GaN����������ת�Ƶ�Cu���� | |
| D�� | Cu��������ķ�Ӧ��CO2+8H++8e-=CH4+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͨ��ˮ�У�F2+H2O�TH++F++HFO | |
| B�� | �������������������Fe3O4+8H+�T2Fe3++Fe2++4H2O | |
| C�� | ��������Һ�еμӹ�����ˮ��Ag++NH3•H2O�TAgOH��+NH4+ | |
| D�� | ��KAl��SO4��2��Һ�е���Ba��OH��2��Һ�����������ʵ������Al3++2SO42-+2Ba2++4OH-�TAlO2-+2BaSO4��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
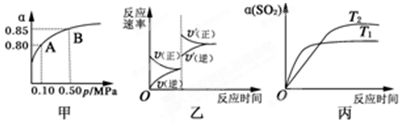
| A�� | ��ͼ���ƶϣ�B��SO2��ƽ��Ũ��Ϊ0.3 mol•L-1 | |
| B�� | ��ͼ���ƶϣ�A���Ӧ�¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ800��L•mol-1�� | |
| C�� | ��ƽ��������������ݻ�����Ӧ���ʱ仯ͼ�������ͼ�ұ�ʾ | |
| D�� | ѹǿΪ0.50 MPaʱ��ͬ�¶���SO2ת�������¶ȹ�ϵ���ͼ����T2��T1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
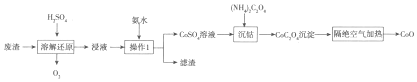
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢ� | B�� | �٢ڢ� | C�� | �ڢۢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com