
| A. | 冰雪融化 | B. | 干冰升华 | C. | 蜡烛燃烧 | D. | 酒精挥发 |
分析 A.冰雪融化过程中只是状态发生改变,没有新物质生成;
B.干冰升华过程中只是状态发生改变,没有新物质生成;
C.蜡烛燃烧过程中有新物质二氧化碳等生成;
D.酒精挥发只是状态发生改变,没有新物质生成.
解答 解:A.冰雪融化过程中只是状态发生改变,没有新物质生成,属于物理变化,故A错误;
B.干冰升华过程中只是状态发生改变,没有新物质生成,属于物理变化,故B错误;
C.蜡烛燃烧过程中有新物质二氧化碳等生成,属于化学变化,故C正确;
D.酒精挥发只是状态发生改变,没有新物质生成,属于物理变化,故D错误.
故选C.
点评 本题考查物理变化与化学变化的区别与联系,难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:选择题

| A. | 若将乙池电解液换成AgNO3溶液,则可以实现在石墨棒上镀银 | |
| B. | 甲池通入CH3OH的电极反应式为CH3OH+6e-+2H2O═CO$\stackrel{2-}{3}$+8H+ | |
| C. | 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 | |
| D. | 甲池中消耗224mL(标准状况下)O2,此时丙池中理论上产生1.16g固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
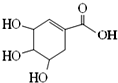
| A. | 分子式为C7H10O5 | |
| B. | 分子中含有3种官能团 | |
| C. | 可发生加成和取代反应 | |
| D. | 在水溶液中羟基和羧基均能电离出氢离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3的摩尔质量为17g | |
| B. | 48gO3含有的臭氧分子数为6.02×1023 | |
| C. | 1mol•L-1NaCl溶液中含1molNa+ | |
| D. | 标准状况下,1molH2O的体积为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水银不是银,而是金属汞 | B. | 纯碱不是碱,而是盐 | ||
| C. | 干冰不是冰,而是固体二氧化碳 | D. | 烧碱不是碱,而是一种常见的盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
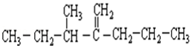 名称为3-甲基-2-丙基-1-戊烯.
名称为3-甲基-2-丙基-1-戊烯.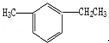 名称为1-甲基-3-乙基苯.
名称为1-甲基-3-乙基苯. 名称为:2,4-二甲基-3-乙基戊烷.
名称为:2,4-二甲基-3-乙基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:
碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵.在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.完成下列填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
| B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
| C | NH3(g) | NO | NO2 | O2 |
| D | S(s) | SO2 | SO3 | O2 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com