
【题目】“异丙苯氧化法”生产丙酮和苯酚的合成路线如下,各反应的原子利用率均为100%。下列说法正确的是
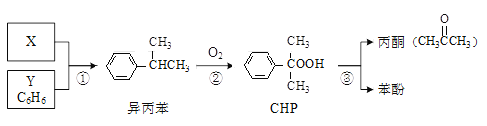
A. X的分子式为C3H8B. Y与异丙苯可用酸性KMnO4溶液鉴别
C. CHP与CH3COOH含有相同的官能团D. 可以用分液的方法分离苯酚和丙酮
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 25℃、101kPa 时,22.4L乙烷中所含共价键数目为6NA
B. 3.2gO2和O3的混合气体中,含氧原子数为0.2NA
C. 12g金刚石含有共价键数目为4NA
D. 1molNaHSO4熔融时电离出的离子总数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____,与钛同周期的元素中,基态原子的未成对电子数与钛相同的元素分别是____(填元素符号)。
(2)在浓的TiCl 3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配合物的化学式为______; 1mol该配合物中含有σ键的数目_______。
(3)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。
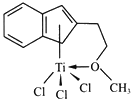
①组成M的元素中,电负性最大的是_________(填名称)。
②M中非金属元素的第一电离能大小顺序_________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(4)金红石(TiO 2)是含钛的主要矿物之一。其晶胞是典型的四方晶系,结构(晶胞中相同位置的原子相同)如图所示。
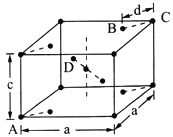
若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为了验证SO2的还原性并测定产生SO2的质量,组装了下图装置。回答下列问题:
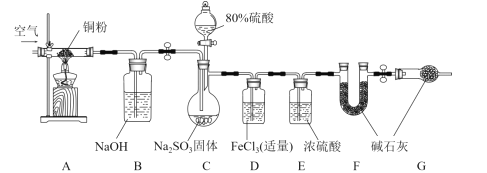
(1)C中发生反应的化学方程式是________,B装置的名称是_________,关于该套装置说法正确的是_________(填标号)。
a 组装仪器、加入药品后检查气密性 b 实验开始和最后时均需要通入空气
c 利用A、B装置是为了减小实验误差 d F、G中的碱石灰可以换为无水CaCl2
(2)甲同学认为很快可以看到D装置的现象,他的依据是_________(用离子方程式表示)。乙同学做实验时发现和甲同学预测的现象不一样,先出现棕红色,经过一段时间后变为浅绿色。于是查阅资料发现反应分为两步:
第一步:![]() (快反应)
(快反应)
第二步:![]() (慢反应)
(慢反应)
如果需要验证第一步反应是快反应,可以事先在D装置中滴加数滴_________试剂,相应的实验现象是________。
(3)学习小组通过实验后D和F装置中的数据来计算SO2的质量。D中加入足量的BaCl2溶液充分反应,经过________操作,测得沉淀为m1g,F的质量差为m2g,C中产生SO2的体积(标准状况下)为_________L。该实验的设计中,仍然存在系统误差的可能原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的捕集、利用与封存(CCUS)是我国能源领域的一个重要战略方向。CO2可转化成有机物实现碳循环。在 2 L 的恒温恒容密闭容器中,充入 2molCO2 和 6molH2,一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),测得 CO2 和 CH3OH(g)的浓度随时间变化如图:
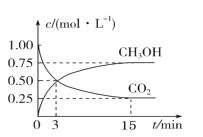
(1)从 3 min 到 15min,υ(H2)=____molL-1min-1;
(2)能说明上述反应达到平衡状态的是_____填编号)。
A. 反应中 CO2 与 CH3OH 的物质的量浓度之比为 1∶1(即图中交叉点)
B. 混合气体的压强不随时间的变化而变化
C. 单位时间内生成 1mol H2,同时生成 1mol CH3OH
D. 混合气体的平均密度不随时间的变化而变化
(3)平衡时 CO2 的转化率为 _____。
(4)平衡混合气体中 CO2(g)和 H2(g)的物质的量之比是 ______。
(5)第 3 分钟时υ正(CH3OH)______第 15 分钟时υ逆(CH3OH)(填“>”、“<” “=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.H2O+Na2O=2NaOHB.2H2O+2F2=4HF+O2
C.2H2O![]() O2↑+2H2↑D.3NO2+H2O=2HNO3+NO
O2↑+2H2↑D.3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:ClO-+CO2+ H2O =HClO+HCO3-
B.硅酸钠溶液与醋酸溶液混合: SiO32-+ 2H+ = H2SiO3↓
C.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH-
D.Ca(ClO)2溶液中通入过量的SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述正确的是
A..由H和Cl形成HCl的过程:![]()
B.常温时,饱和NaClO溶液的pH约为11:ClO-+H2O=HClO+OH-
C.苯酚和甲醛在一定条件下反应能生成酚醛树脂: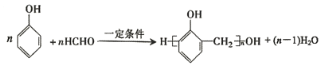
D.电解饱和食盐水的反应:2Cl-+2H+![]() Cl2↑+H2↑
Cl2↑+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过以下装置测定M样品(只含Fe、Al、Cu)中各成分的质量分数。取两份质量均为m g的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为V1 mL和V2 mL(已折算到标准状况下)。

(1)写出实验1中发生反应的离子方程式:______________________________。
(2)实验1装置中小试管的作用是___________________________________________________。
(3)对于实验2,平视读数前应依次进行的两种操作是:①___________________②___________________。
(4)M样品中铜的质量的数学表达式为(用m 、V1和V2 表示):__________________________。
(5)实验1进行实验前,B瓶中水没有装满,使测得气体体积____________ (填“偏大”、“偏小”或“无影响”,下同);若拆去实验2中导管a,使测得气体体积___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com