
分析 (1)①发生反应:4FeCO3+O2$\frac{\underline{\;加热\;}}{\;}$2Fe2O3+4CO2,根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减,构造目标热化学方程式;
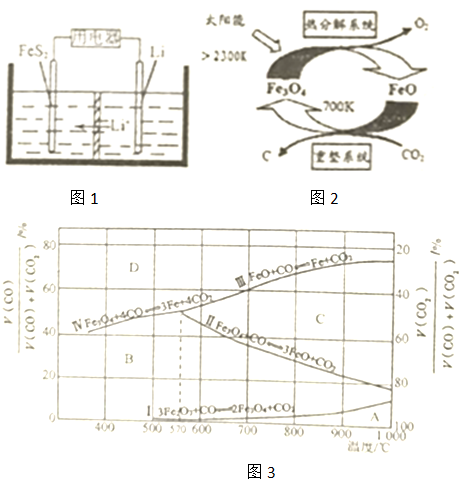
②电池放电时的总反应为:4Li+FeS2═Fe+2Li2S,正极发生还原反应,FeS2获得电子生成Fe、S2-;
(2)①反应2Fe3O4$\frac{\underline{\;\;△\;\;}}{\;}$6FeO+O2↑中O元素化合价由-2价升高到0价,结合元素化合价以及方程式计算;
②由示意图可知,重整系统中CO2和FeO反应生成Fe3O4和C;
(3)①800℃时,混合气体中CO2体积分数为40%时,图象分析可知Fe2O3用CO还原得到氧化亚铁和一氧化碳;
②A.由图可知,FeO在C区稳定,对应的温度高于570℃;
B.铁元素的质量分数由高到低为:Fe>FeO>Fe3O4>Fe2O3,对于反应II知,升高温度时,CO2的质量分数减小,即升温平衡逆向移动,FeO转化成Fe3O4,F铁元素的质量分数减小,所以含量不仅与T有关,还与CO气体的比例有关;
C.分离CO2可使四个反应的平衡均正向移动,有利于Fe含量的增加.
解答 解:(1)①发生反应:4FeCO3+O2$\frac{\underline{\;加热\;}}{\;}$2Fe2O3+4CO2,
已知:①4Fe(s)+3O2(g)═2Fe2O3(s)△H=-1648kJ/mol
②C(s)+O2(g)═CO2(g)△H=-393kJ/mol
③2Fe(s)+2C(s)+3O2(g)═2FeCO3(s)△H=-1480kJ/mol
根据盖斯定律,①-③×2+②×④可得4FeCO3(s)+O2(g)=2Fe2O3(s)+4CO2(g),△H=-1648kJ/mol-2×(-1480kJ/mol)+4×(-393kJ/mol)=-260kJ/mol,
故反应热化学方程式为:4FeCO3(s)+O2(g)=2Fe2O3(s)+4CO2(g)△H=-260kJ/mol,
故答案为:4FeCO3(s)+O2(g)=2Fe2O3(s)+4CO2(g)△H=-260kJ/mol;
②电池放电时的总反应为:4Li+FeS2═Fe+2Li2S,正极发生还原反应,FeS2获得电子生成Fe、S2-,正极电极反应式为:FeS2+4e-=Fe+2S2-,
故答案为:FeS2+4e-=Fe+2S2-;
(2)①反应2Fe3O4$\frac{\underline{\;\;△\;\;}}{\;}$6FeO+O2↑中O元素化合价由-2价升高到0价,由方程式可知,2molFe3O4参加反应,生成1mol氧气,转移4mol电子,则每分解lmolFe3O4转移电子的物质的量为2mol,
故答案为:2mol;
②由示意图可知,重整系统中CO2和FeO反应生成Fe3O4和C,反应的方程式为6FeO+CO2═2Fe3O4+C,
故答案为:6FeO+CO2═2Fe3O4+C;
(3)①800℃时,混合气体中CO2体积分数为40%时,由图可知,“800℃、CO2体积分数为40%”时,在C区,此时为FeO的稳定区域,故产物为FeO,Fe2O3用CO还原得到氧化亚铁和一氧化碳,反应的化学方程式为:Fe2O3+CO$\frac{\underline{\;800℃\;}}{\;}$2FeO+CO2,
故答案为:Fe2O3+CO$\frac{\underline{\;800℃\;}}{\;}$2FeO+CO2;
②A.由图可知,FeO在C区稳定,对应的温度高于570℃,故A正确;
B.铁元素的质量分数由高到低为:Fe>FeO>Fe3O4>Fe2O3,对于反应II知,升高温度时,CO2的质量分数减小,即升温平衡逆向移动,FeO转化成Fe3O4,F铁元素的质量分数减小,所以含量不仅与T有关,还与CO气体的比例有关,故B错误;
C.分离CO2可使四个反应的平衡均正向移动,有利于Fe含量的增加,故C正确,
故答案为:AC.
点评 本题较为综合,涉及氧化还原、化学平衡移动以及原电池反应等知识,考查了学生分析问题、解决问题的能力,题目难度中等.注意电极正负极的判断以及反应式的书写,注意燃料电池的负极上是燃料发生失电子的氧化反应.


科目:高中化学 来源: 题型:填空题
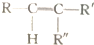 $\stackrel{高锰酸钾酸性溶液}{→}$R-COOH+
$\stackrel{高锰酸钾酸性溶液}{→}$R-COOH+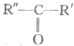
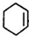 ,HOOC(CH2)4COOH.
,HOOC(CH2)4COOH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
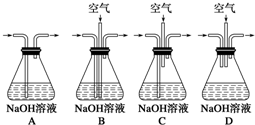 实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中加热,使之反应完全,通过蒸发、结晶得到硫酸铜晶体.
实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中加热,使之反应完全,通过蒸发、结晶得到硫酸铜晶体.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 温度℃ | 400 | 500 | 830 | 1000 |
| 平均常数K | 10 | 9 | 1 | 0.6 |
| A. | 上述反应中正反应是吸热反应 | |
| B. | 该反应的化学平衡常数表达式为K=$\frac{\{c({H}_{2})•c(C{O}_{2})\}}{\{c(CO)•c({H}_{2}O)\}}$ | |
| C. | 该反应在400℃时达平衡状态,若升高温度,则正反应速率减小,逆反应速率增大 | |
| D. | 在830℃,2L的密闭容器中,冲入1molCO、5molH2O(g)、3molCO2和2molH2发生上述反应,在达到平衡前V(正)<V(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定时可用氯水代替过氧化氢氧化甲醛 | |
| B. | 足量H2O2氧化1molHCHO时放出的热量-定是①的2倍 | |
| C. | 上述方法测定甲醛含量时,如果H2O2过量,会导致甲醛含量的测定结果偏高 | |
| D. | H2O2氧化甲醛(反应①)和氧化甲酸的原理相同,氧化等量甲醛和甲酸时转移电子的数目也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制催化剂的材料 | B. | 耐高温、耐腐蚀的合金材料 | ||
| C. | 半导体材料 | D. | 制农药的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式为:C2H4 | |
| B. | S2-的结构示意图: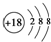 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | NH4Cl的电子式为: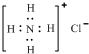 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
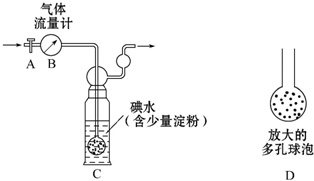
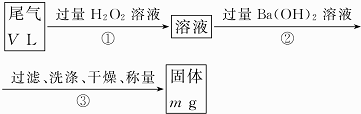
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
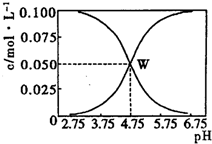 25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述不正确的是( )
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述不正确的是( )| A. | 由题给图示可求出25℃时醋酸的电离平衡常数Ka=10-4.75 | |
| B. | W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | |
| C. | pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol•L-1 | |
| D. | 向W点所表示的1.0 L溶液中通入0.05 mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH))+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com