
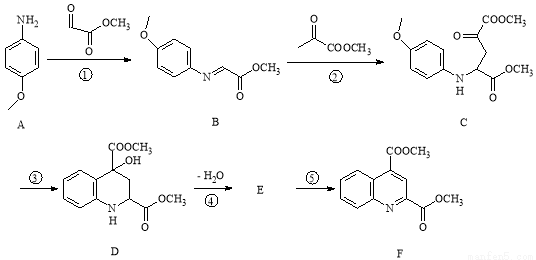
(14分)药物F具有抗肿瘤、降血压、降血糖等多种生物活性,其合成路线如下:
已知: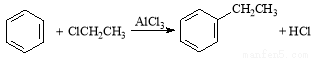
(1)原料A中含氧、含氮的官能团名称是 、 。
(2)写出中间产物E的结构简式 。
(3)反应②、⑤的反应类型是 、 。
(4)物质B有多种同分异构体,写出满足下列条件的一种同分异构体的结构简式 。
①属于α-氨基酸
②苯环上有两种一氯代物
③能发生银镜反应
④核磁共振氢谱显示其有7种不同化学环境的氢原子
(5)以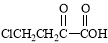 和苯、乙醇为原料,可合成
和苯、乙醇为原料,可合成 ,写出合成流程
,写出合成流程
图(无机试剂任用)。合成流程图示例如下:
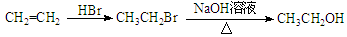
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列表述正确的是
A.将 0.1 mol·L-1HCl溶液加热到100℃,溶液的pH仍为1
B.将pH=4的醋酸溶液加水稀释后,溶液中所有离子的浓度均降低
C.常温下,若1mLpH=1的盐酸与10mLNaOH溶液混合后溶液的pH=7,则NaOH溶液的pH=12
D.在滴有酚酞试液的氨水中,加入NH4Cl至溶液呈无色,此时溶液一定显中性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
氮化钠(Na3N)晶体熔融时能导电。下列描述正确的是
A.构成晶体的两种微粒电子层结构相同
B.构成晶体的两种微粒半径相等
C.构成晶体的两种微粒的核外电子能量相同
D.构成晶体的两种微粒的电子层数不同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
假蜜环菌甲素可作为药物用于治疗急性胆道感染病毒性肝炎等疾病,其结构简式如下。下列对假蜜环菌甲素的性质叙述正确的是
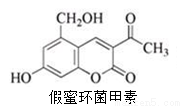
A.假蜜环菌甲素可以发生消去反应
B.1 mol假蜜环菌甲素可与 6 mol H2 发生加成反应
C.假蜜环菌甲素可与 NaOH 溶液在加热条件下发生水解反应
D.假蜜环菌甲素既能与Na反应生成H2,又能与NaHCO3反应生成CO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
某药物中间体的合成路线如下。下列说法正确的是
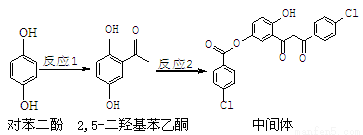
A.对苯二酚在空气中能稳定存在
B.1 mol该中间体最多可与11 mol H2反应
C.2,5-二羟基苯乙酮能发生加成、水解、缩聚反应
D.该中间体分子中含有1个手性碳原子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
用下列实验装置进行相应实验,能达到实验目的的是
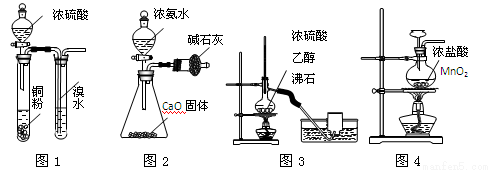
A.用图1所示装置验证浓硫酸具有强氧 化性
化性
B.用图2所示装置制取干燥的NH3
C.用图3所示装置制取并收集乙烯
D.用图4所示装置制取Cl2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三4月质量检查理综化学试卷(解析版) 题型:填空题
[化学—物质结构与性质〕(13分)硅、锗、磷化锢、氮化镓、聚丙烯睛都是半导体材料。
(1)基态锗(Ge)原子的核外电子排布式为 。
(2)聚丙烯睛由丙烯睛(CH2=CH-CN)聚合而成。丙烯睛分子中所有原子都在同一平面上,则丙烯睛分子中,碳原子的杂化轨道类型有 ,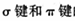 的个数比为 。
的个数比为 。
(3)(CH3)3Ga、(CH3CH2)3Ga是制取氮化稼的常见镓源,常温常压下均为无色透明的液体。下列说法正确的是 (填标号)。
A.(CH3)3Ga晶体属于分子晶体
B.(CH3)3Ga中所含化学键都是极性键
C.(CH3CH2)3Ga晶体中含有氢键
D.(CH3CH2)3Ga中所有原子都达到稀有气体的稳定结构
(4)氮化稼(GaN)的晶体结构如左下图所示。该晶体中 (填“有”或“无”)配位键存在,判断的依据是
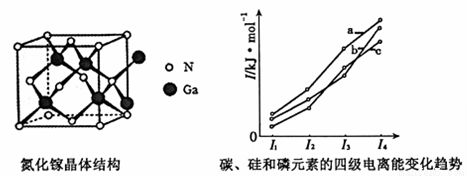
(5)上图表示碳、硅和磷元素的四级电离能变化趋势,其中表示磷的曲线是 (填标号)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高三3月教学质量监测理综化学试卷(解析版) 题型:实验题
(13分)钠、钾的碘化物在生产和科学实验中有十分重要的应用。工业利用碘、NaOH和铁屑为原料可生产碘化钠,其生产流程如下:

(1)NaOH溶液和碘反应时需要严格控制温度,如果温度过低,会生成碘的低价副产品NaIO。若NaOH溶液和碘反应时所得溶液中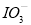 与IO-的物质的量之比为1 :1,则该反应的离子方程式为______________。
与IO-的物质的量之比为1 :1,则该反应的离子方程式为______________。
(2)生产流程中加入过量铁屑的目的是_____________,过滤所得固体中除剩余铁屑外,还有红褐色固体,则加入铁屑时发生反应的化学方程式是_________________________。
(3)溶液2中除含有H+外,一定含有的阳离子是_____________;试设计实验证实该金属阳离子的存在__________________________。
(4)溶液2经一系列转化可以得到草酸亚铁晶体(FeC2O4·2H2O),称取3.60 g草酸亚铁晶体(相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示:

①分析图中数据,根据信息写出过程Ⅰ发生的化学方程式_______________________。
②300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com