
【题目】无色孔雀石绿(结构简式如图所示)曾被用作水产养殖业的杀虫剂(鱼药)。因为具有潜在致癌性,已被禁止用作鱼药。下列关于无色孔雀石绿的叙述中,正确的是
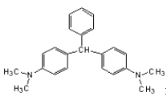
A. 分子中所有的碳原子可能在同一平面上
B. 无色孔雀石绿属于烃的衍生物
C. 无色孔雀石绿可与溴水中的溴发生加成反应
D. 在一定条件下,1mol无色孔雀石绿可以和9mol氢气发生加成反应
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源。下图是从海水中提取某些原料的流程图。

下列有关说法正确的是( )
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.工业上通过氯碱工业制取金属钠
C.从第③步到第⑤步的目的是浓缩、富集溴单质
D.第②步的反应条件是高温加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成治疗高血压药物奈必洛尔的重要中间体,其部分合成路线图如下(Ph代表苯基):
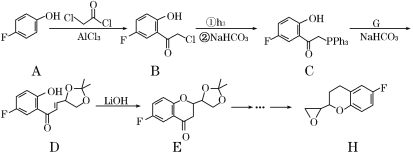
(1)化合物C的含氧官能团名称为________、________。
(2)B→C的反应类型是________。
(3)写出A→B的化学反应方程式________。
(4)C→D的转化中,反应物G的分子式为C6H10O3,生成物除D外还有Ph3P=O,则G的结构简式为_________
(5)写出同时满足下列条件的B的一种同分异构体的结构简式________。
Ⅰ.分子中含有一个酯基和一个手性碳原子,有4种化学环境不同的氢;
Ⅱ.不能发生银镜反应;
Ⅲ.能发生水解反应,且其中一种水解产物能与FeCl3溶液发生显色反应。
(6)已知:
①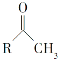
![]() RCOONa
RCOONa
②![]()
![]()
![]()
化合物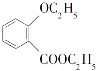 是一种重要的有机合成中间体,请写出以苯酚、乙醇和
是一种重要的有机合成中间体,请写出以苯酚、乙醇和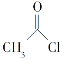 为原料制备该化合物的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
H2C===CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳单质及其化合物有广泛的应用。
(1)碳的同素异性体金刚石、石墨和C60晶体中,能溶于有机溶剂的是___,原因是_______。
(2)CH3COCH=CHCH3分子中,C原子所采取的杂化类型有____________。
(3)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图所示,图中用虚线标出了石墨的一个六方晶胞。该晶胞中含有的碳原子数为_____个。
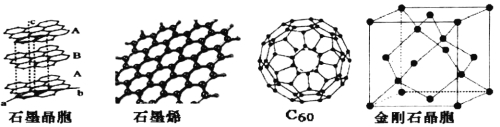
(4)石墨烯是一种由单层碳原子构成的平面结构新型碳材料,如图所示。1mol石墨烯中含有的六元环个数为______,下列有关石墨烯说法正确的是________
a.晶体中碳原子间全部是碳碳单键
b.石墨烯中所有碳原子可以处于同一个平面
c.从石墨中剥离得到石墨烯需克服分子间作用力
(5)石墨烯可转化为C60,C60的结构如图所示,该分子是由五边形和六边形构成的球体,其中五边形有12个,六边形有________个。
(6)金刚石晶胞如图所示,则金刚石晶胞中原子的配位数为_____,原子空间利用率为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为______,该能层具有的原子轨道数为_______。
②LiBH4由Li+和BH4-构成,BH4-的立体结构是_________,B原子的杂化轨道类型是________。
Li、B、H元素的电负性由大到小排列顺序为________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径Li+_______H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:

M是________ (填元素符号)。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为________,NaH的理论密度是___________g·cm-3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。

(1)A的结构式为______。
(2)B分子中的官能团名称是______,C的名称为______。
(3)写出下列反应的化学方程式:
①__ ___。
③___ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”。凡具有一个手性碳原子的化合物一定具有光学活性。例如,有机物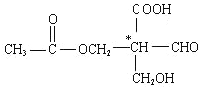 含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
A、与NaOH溶液共热 B、与银氨溶液共热
C、与金属钠反应 D、与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙烯为原料合成环状化合物 E(C4H4O4)的流程如下。
![]()
请回答下列问题:
(1)E 的结构简式是_______________;C 中所含官能团的名称是____________。
(2)在乙烯的同系物中,所有碳原子一定共平面且碳原子数最多的分子的结构简式是__________,名称(系统命名)是______________。
(3)反应①⑤中,属于取代反应的是_______(填写编号)。
(4)写出反应②的化学方程式______________ 。
(5)F是E的同分异构体,且1 mol F与足量的 NaHCO3溶液反应可放出2mol CO2气体,请写出符合条件的F的所有的结构简式______________ 。
(6)参照上述合成路线的表示,设计以乙烯为原料制备乙二醇的最简合成路线:
__________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中含量最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的+1价阳离子的核外有3个电子层且各层均充满。
回答下列问题:
(1)W+的价电子排布式为 。
(2)Y2X2分子中Y原子轨道的杂化类型为 ,1mol Y2X2含有σ键的数目为 。
(3)化合物ZX3的沸点比化合物YX4的高,其主要原因是 。
(4)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 。
(5)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是 ,它可与浓盐酸发生非氧化还原反应,生成配合物H2WCl3,反应的化学方程式为 。在晶胞中最近的2个原子距离是apm,晶胞的密度是_____________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
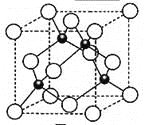
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com