
| A. | 硫酸铁溶液(硫酸亚铁):通入足量氯气,充分反应后加热,使多余氯气逸出 | |
| B. | 苯(苯酚):加入足量的浓溴水,充分振荡,静置分层后分离 | |
| C. | CO2(SO2):通入盛有Na2CO3溶液的洗气瓶 | |
| D. | Mg(OH)2:放入水中调成浆状,加入足量MgCl2溶液,充分搅拌,过滤,沉淀用蒸馏水洗涤 |
分析 A.通入足量氯气,可氧化亚铁离子,但引入新杂质氯离子;
B.溴、三溴苯酚均易溶于苯;
C.二者均与碳酸钠溶液反应;
D.加入足量MgCl2溶液,有利于生成Mg(OH)2.
解答 解:A.通入足量氯气,可氧化亚铁离子,但引入新杂质氯离子,应选过氧化氢除杂,故A错误;
B.溴、三溴苯酚均易溶于苯,不能除杂,应选NaOH溶液、分液除杂,故B错误;
C.二者均与碳酸钠溶液反应,应通入盛有NaHCO3溶液的洗气瓶,故C错误;
D.加入足量MgCl2溶液,有利于生成Mg(OH)2,则充分搅拌,过滤,沉淀用蒸馏水洗涤即可得到Mg(OH)2,故D正确;
故选D.
点评 本题考查物质分离提纯,为高频考点,把握物质的性质、发生的反应及混合物分离方法为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
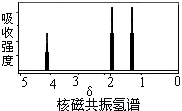
| A. | CH3COOCH2CH3 | B. | CH3CH=CHCH3 | C. | CH3CH2CH3 | D. | CH3CHOHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
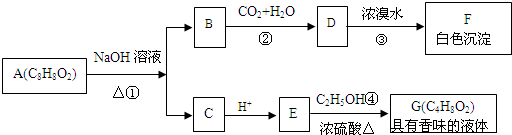
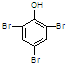 ;
;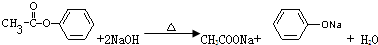 ;
;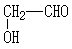 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
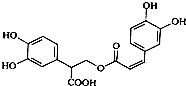
| A. | 迷迭香酸属于芳香烃 | |
| B. | 1mol迷迭香酸最多能和含6mol H2发生加成反应 | |
| C. | 迷迭香酸可以发生水解反应、消去反应和酯化反应 | |
| D. | 1mol迷迭香酸最多能和含6mol NaOH的水溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
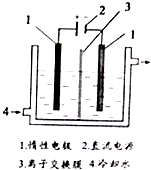 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中物质变化的实质是旧化学键的断裂和新化学键的形成 | |
| B. | 离子化合物中一定有金属元素和非金属元素 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 共价化合物中各原子都一定满足最外层8电子稳定结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com