
【题目】下列说法正确的是
A.盐类物质一定含有金属阳离子
B.蔗糖、NH3、液态HCl均为非电解质
C.能导电的物质不一定属于电解质
D.非金属氧化物一定是酸性氧化物
科目:高中化学 来源: 题型:
【题目】已知丙酮(C3H6O)通常是无色液体,易溶于水,密度小于1 gmL﹣1 , 沸点约为55℃.要从水与丙酮的混合物中将丙酮分离出来,下列方法中最为合理的是( )
A.蒸馏
B.分液
C.过滤
D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.A~D是四种烃分子的球棍模型(如图)
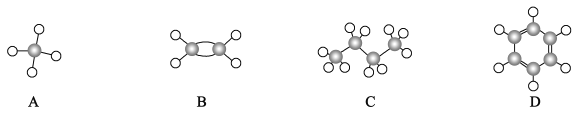
(1)所有原子一定共平面的是______(填序号)
(2)能使酸性高锰酸钾溶液褪色的物质是_____ (填序号)
(3)D与浓硝酸和浓硫酸共热的化学方程式______。
II.某些有机物的转化如下图所示。已知:A是营养物质之一,米饭、馒头中富含A,在酸性条件下水解的最终产物是B。C是白酒的主要成分,D的水溶液能使紫色石蕊试液变红。
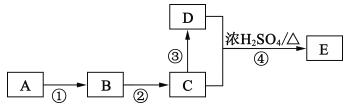
(4)C中官能团的名称为______;反应③的反应类型为______,反应④的化学方程式为______。
(5)反应④中,D断裂的化学键是_______ (填“C一H”、“O一H”或“C一O”)
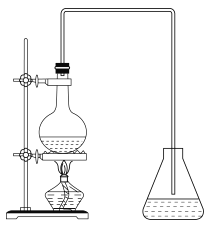
(6)实验室由反应④制备E的装置如图所示。烧瓶中依次加入C、浓硫酸、D和碎瓷片,锥形瓶中加入的是饱和碳酸钠溶液,实验结束后振荡锥形瓶内液体,看到有气泡产生,产生气泡的原因是__________(用离子方程式表示),将锥形瓶中的液体分离的方法是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据框图分析,下列说法不正确的是
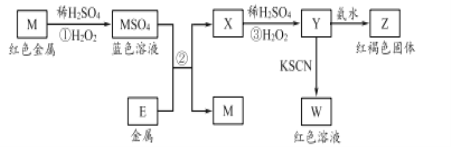
A. 我国是世界上最早使用反应②冶炼金属M的国家
B. M2+的氧化性比E2+的氧化性强
C. 在反应③中若不加稀硫酸,可能观察到红褐色沉淀
D. 在反应①中稀硫酸既表现出氧化性又表现出酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、D、E、F是原子序数依次增大的六种常见元素。E的单质在Z2中燃烧的产物可使品红溶液褪色。F和Z元素形成的化合物F3Z4具有磁性。X的单质在Z2中燃烧可生成XZ和XZ2两种气体。D的单质是一种金属,该金属在XZ2中剧烈燃烧生成黑、白两种固体。请回答下列问题:
(1)F元素在周期表中的位置是________,Y的单质分子的结构式为__________,DZ的电子式为________,DZ化合物中离子半径较大的是________(填离子符号)。
(2)X元素形成的同素异形体的晶体类型可能是________(填序号)。
①原子晶体 ②离子晶体 ③金属晶体 ④分子晶体
(3)X、Y、Z形成的10电子氢化物中,X、Y的氢化物沸点较低的是(写化学式):__________;Y、Z的氢化物分子结合H+能力较强的是(写化学式)________。
(4)下列可作为比较D和Na金属性强弱的依据是________。(填序号)
a.测两种元素单质的硬度和熔、沸点
b.比较两元素最高价氧化物对应的水化物溶液的碱性强弱
c.比较两种元素在氯化物中化合价的高低
d.比较单质与同浓度盐酸反应的剧烈程度
(5)Y的氢化物和Z的单质在一定条件下反应生成Z的氢化物(产物之一),该反应的方程式为___________。
(6)有人建议将氢元素排在元素周期表的ⅣA族,请你从化合价的角度给出一个理由__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应H2(g)+I2(g)![]() 2HI(g)在温度和容积不变的条件下进行。能说明反应达到平衡状态的叙述是( )
2HI(g)在温度和容积不变的条件下进行。能说明反应达到平衡状态的叙述是( )
A. c(H2)=c(I2) B. H2的消耗速率等于HI的分解速率
C. 容器内气体的颜色不再变化 D. 容器内压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用与盐类的水解无关的是
A. 明矾用于净水
B. 次氯酸钠常用作消毒剂
C. FeCl3溶液滴入沸水中制Fe(OH)3胶体
D. 用碳酸氢钠和硫酸铝两种溶液可制成泡沫灭火剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com