
| A. | 配制过程只需要三种仪器即可完成 | |
| B. | 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 需要称量的NaClO固体的质量为140 g |
分析 A.配制过程中需要用到天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管等;
B.容量瓶中有水,对溶液的体积无影响;
C.由于NaClO易吸收空气中的H2O、CO2而变质,所以商品NaClO可能部分变质导致NaClO减少;
D.容量瓶的规格没有480mL,应选取500 mL的容量瓶进行配制.
解答 解:A.需用托盘天平、药匙称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,故A错误;
B.容量瓶中有水,对溶液的体积无影响,所以经洗涤干净的容量瓶不必烘干后再使用,故B错误;
C.由于NaClO易吸收空气中的H2O、CO2而变质,所以商品NaClO可能部分变质导致NaClO减少,配制的溶液中溶质的物质的量减小,则溶液的物质的量浓度偏小,故C正确;
D.应选取500 mL的容量瓶进行配制,然后取出480mL即可,所以需要NaClO的质量:500mL×1.19 g•cm-3×25%=148.75g,应该用托盘天平称量148.8g次氯酸钠,故D错误;
故选C.
点评 本题主要溶液配制的步骤、仪器以及误差分析等知识,题目难度中等,注意注意配制一定浓度的溶液方法,D为易错点,需要明确计算溶质的质量时,溶液的体积按500mL计算.


科目:高中化学 来源: 题型:解答题
 ).则1mol的该有机物跟足量的金属钠反应可以产生1.5molH2,1mol该有机物可以跟1molNaHCO3反应,1mol该有机物可以跟2molNaOH反应.
).则1mol的该有机物跟足量的金属钠反应可以产生1.5molH2,1mol该有机物可以跟1molNaHCO3反应,1mol该有机物可以跟2molNaOH反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
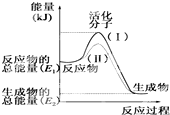 请认真观察如图,然后回答问题:
请认真观察如图,然后回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①② | C. | ②④ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.050 mol | B. | 0.060 mol | C. | 0.100 mol | D. | 0.200 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 由于乳酸(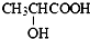 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 | |
| C. | 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 | |
| D. | 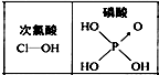 由如图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用高纯度的锌粒 | B. | 滴加几滴硫酸铜溶液 | ||
| C. | 使用浓H2SO4 | D. | 使用浓HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com