
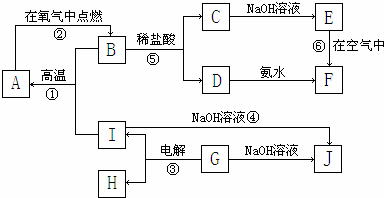
分析 G为主族元素的固态氧化物,电解G得到I和H,G能和氢氧化钠溶液反应生成J,工业上用电解氧化铝的方法冶炼铝,则G是Al2O3,I能和氢氧化钠溶液反应生成J,则I是Al,J是NaAlO2,H是O2,Al和B能在高温下反应生成A,A能在H中燃烧生成B,铝在高温下能发生铝热反应,则B是金属氧化物,A是金属单质,B和盐酸反应生成C和D,C和氢氧化钠反应生成E,D和氨水反应生成F,E在空气中反应生成F,说明E不稳定,易被氧气氧化,且A、B、C、D、E、F六种物质中均含同一种元素,则A是Fe,B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2,F为Fe(OH)3,结合对应单质、化合物的性质解答该题.
解答 解:G为主族元素的固态氧化物,电解G得到I和H,G能和氢氧化钠溶液反应生成J,工业上用电解氧化铝的方法冶炼铝,则G是Al2O3,I能和氢氧化钠溶液反应生成J,则I是Al,J是NaAlO2,H是O2,Al和B能在高温下反应生成A,A能在H中燃烧生成B,铝在高温下能发生铝热反应,则B是金属氧化物,A是金属单质,B和盐酸反应生成C和D,C和氢氧化钠反应生成E,D和氨水反应生成F,E在空气中反应生成F,说明E不稳定,易被氧气氧化,且A、B、C、D、E、F六种物质中均含同一种元素,则A是Fe,B为Fe3O4,C为FeCl2,D为FeCl3,E为Fe(OH)2,F为Fe(OH)3,
(1)A、B、C、D、E、F六种物质中所含的同一种元素是Fe元素,铁元素位于第四周期第Ⅷ族,故答案为:第四周期、第Ⅷ族;
(2)反应①是高温下铝和四氧化三铁反应生成氧化铝和铁,反应方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe,
故答案为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe;
(3)反应④是铝和氢氧化钠反应生成偏铝酸钠和氢气,反应方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)G是Al2O3,电解氧化铝,阳极发生3O22--6e-=3O2↑;阴极发生2Al3++6e-=2Al,故答案为:3O22--6e-=3O2↑;2Al3++6e-=2Al;
(5)铝热反应和燃烧反应都是放热反应,故答案为:①②.
点评 本题考查无机物的推断,为高频考点,侧重于学生的分析能力的考查,题目难度较大,注意推断的关键点:①G为主族元素的固态氧化物,在电解条件下生成I和H,能与NaOH溶液反应,说明G为Al2O3,②C、D分别和碱反应生成E、F,则说明E、F都为氢氧化物,E能转化为F,应为Fe(OH)2→Fe(OH)3的转化.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
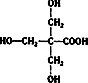 .
.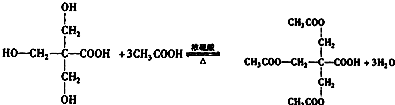 .
.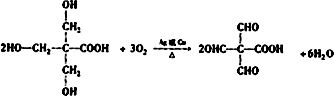 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H原子形成1molH-H键要吸收热量 | |
| B. | 化学变化中的能量变化的大小与反应物的质量多少无关 | |
| C. | 酸与碱的稀溶液发生中和反应生成1molH2O时所释放的热量称为中和热 | |
| D. | 锌锰干电池中碳棒是负极,锌片是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCO2 | |
| B. | 标准状况下44.8LH2 | |
| C. | 32gO2 | |
| D. | 1L 1mol/L的碳酸钠溶液中含有的溶质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 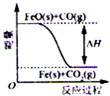 | B. |  | C. | 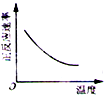 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
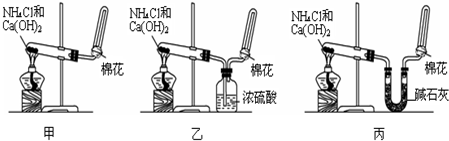
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水煤气,电能是一级能源 | |
| B. | 天然气,水力是二级能源 | |
| C. | 核能,煤,石油符合未来新能源标准 | |
| D. | 太阳能,生物质能,风能,氢能符合未来新能源标准 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com