
ȡ8.34 g FeSO4��7H2O��Ʒ���ȣ���������ˮ���̵���������(��Ʒ�������¶ȱ仯������)����ͼ��ʾ�������������в���ȷ���ǣ� ��
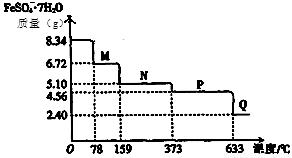
A���¶�Ϊ78��ʱ��������M�Ļ�ѧʽΪFeSO4?4H2O
B���¶�Ϊl59��ʱ��������N�Ļ�ѧʽΪFeSO4?H2O
C���ڸ������������£�N�õ�P�Ļ�ѧ����ʽΪ��FeSO4  FeO+SO3��
FeO+SO3��
D������P��������������650�棬�õ�һ�ֹ�������Q��ͬʱ��������ɫ�������ɣ�Q�Ļ�ѧʽΪFe2O3
C
��������
���������A. 8.34 g FeSO4��7H2O���ֽ��ΪFeSO4?4H2O������������(8.34 g��278g/mol)��224g/mol=6.72g����ͼ����ϣ���ȷ��B�����¶�Ϊl59��ʱ�������Ĺ�������N�Ļ�ѧʽΪFeSO4?H2O������������(8.34 g��278g/mol)��170g/mol=5.10g����ͼ���Ǻϣ���ȷ��C������N�Ļ�ѧʽ��FeSO4?H2O��N�ֽ����õ�FeSO4�����̬�����ǣ�(8.34 g��278g/mol)��152g/mol=4. 56g��������Pʱ���ʵĻ�ѧʽ��FeSO4���ڸ������������£�N�õ�P�Ļ�ѧ����ʽΪ��FeSO4?H2O FeSO4 + H2O ������D������P��������������650�棬�õ�һ�ֹ�������Q��ͬʱ��������ɫ�������ɣ���Q�Ļ�ѧʽΪFe2O3�������Ԫ���غ�ɵ������ǣ�[(8.34 g��278g/mol)��2]��160g/mol=2.40g,��ͼ���Ǻϣ���ȷ��
FeSO4 + H2O ������D������P��������������650�棬�õ�һ�ֹ�������Q��ͬʱ��������ɫ�������ɣ���Q�Ļ�ѧʽΪFe2O3�������Ԫ���غ�ɵ������ǣ�[(8.34 g��278g/mol)��2]��160g/mol=2.40g,��ͼ���Ǻϣ���ȷ��
���㣺�����̷����ȷֽ�������¶ȵĹ�ϵ��֪ʶ��


 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������е�̼ԭ��������ԭ�ӵĽ�Ϸ�ʽһ����ͨ���Ǽ��Լ� | B�� ������������11��̼ԭ�Ӵ���ͬһƽ�� ������������11��̼ԭ�Ӵ���ͬһƽ�� | C������ϩ��ʹ��ˮ��ɫ | D����֬������ụΪͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и����ڶ���ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ������
��8�֣���֪�����³�ѹ�£�D��E��F��I��JΪ���壻 1molE�뺬1molF��ˮ��Һǡ�÷�Ӧ����B��B��һ�ֳ����Ļ��ʡ����� ֮��������ͼ��ʾת����ϵ�����ַ�Ӧ�����ɵ�ˮ����ȥ����
֮��������ͼ��ʾת����ϵ�����ַ�Ӧ�����ɵ�ˮ����ȥ����

�Իش��������⣺
��1����֪A��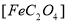 ��C��FeԪ�ؾ�Ϊ��2�ۣ���
��C��FeԪ�ؾ�Ϊ��2�ۣ��� ��̼Ԫ�صĻ��ϼ�Ϊ______
��̼Ԫ�صĻ��ϼ�Ϊ______
��2��B�Ļ�ѧʽΪ___________________��
��3��д����Ӧ�۵Ļ�ѧ����ʽ _______________________ _____��
��4��д����������H��K��ϡ��Һ��Ӧ�����ӷ���ʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��13�֣�ͭ���仯�����������������й㷺Ӧ�ã�ͭ�ڻ������еij������ϼ���+l��+2����֪Cu2O��ϡ���ᷴӦ����Һ����ɫ��
��1����ҵ�Ͽ���Cu2S+O2 2Cu+SO2��Ӧ��ȡ��ͭ������32gCu2S����ʱ������ת����Ŀ�� ��
2Cu+SO2��Ӧ��ȡ��ͭ������32gCu2S����ʱ������ת����Ŀ�� ��
��2��������ͭ˿����������ϡ�����У��¶ȿ�����50�棬����H2O2����Ӧһ��ʱ������µ�60�棬�ٷ�Ӧһ��ʱ�����Ƶ�����ͭ���¶ȿ�����50��-60�������ԭ����˼ӿ췴Ӧ�����⣬���� ����CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ���ȣ�����CuCl����,д������CuCl�����ӷ���ʽ ��
��3��ijС��ͬѧ����ͭ��Ũ���ᷴӦ��ʵ��ʱ������ͭƬ�����к�ɫ�������ɡ�
�ټ�ͬѧ���룺��ɫ������δ���ü��ܽ������CuO, �������û�ѧ����ʽ��ʾΪ��
Cu + H2SO4
����ͬѧ��Ϊ����ɫ�����CuO����ܺ���Cu2S��CuS.�����ɿ����� ������ĸ��
a��Cu2S��CuS���Ǻ�ɫ��
b��ͭ��Ũ�����ڼ��������·�Ӧ�������ܷų�O2
c��Ũ��������������ͭ�ǻ�ԭ����Cu�Ļ��ϼ�������S�Ļ��ϼ��½��ж��ֿ���
��4������Cu��Cu2O��CuO��ɵĻ�����У�����1 L 0.6 mol/L HNO3��Һǡ��ʹ������ܽ⣬ͬʱ�ռ���2240 mL NO���壨��״������Cu2O��ϡ���ᷴӦ�����ӷ���ʽ���������������������������������� �����������������������H2���Ȼ�ԭ�����õ����������Ϊ�������� g����������к�0.1 mol Cu�����û������ϡ�����ַ�Ӧ����������H2SO4�����ʵ���Ϊ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij������һҺ�����ʱ��ƽ��ʱ����Ϊnml,����ʱ����Ϊxml,����ʱ����Ϊyml����y>n>x�������õ�����������
A����Ͳ B����ʽ�ζ��� C����ʽ�ζ��� D������ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣���1����100����������Ϊ10%��NaOH��Һ��50����������Ϊ20%��NaOH��Һ��Ϻ�ˮϡ������Һ���Ϊ500ml����ϡ�ͺ�NaOH�����ʵ���Ũ��Ϊ
��2����BaCl2��NaCl�Ļ����Һa L���������ֳ����ݡ�һ�ݵμ�ϡ���ᣬʹBa2+ ��ȫ��������һ�ݵμ�AgNO3��Һ��ʹCl�� ��ȫ��������Ӧ������x mol H2SO4��y mol AgNO3���ݴ˵�֪ԭ�����Һ�е�c(Na+)Ϊ mol��L-1
��3��ij��������X�����ȷֽ�3X��A+2B+3C�������Ϊ���壬������������������ͬ����������������ܶ�Ϊ22 ����X�����ԭ������Ϊ
��4����״���£���15 LO2ͨ��10LH2��CO�Ļ�����У����ȼ�ո���ָ�����״��
����ʣ����������Ϊ15 L����ԭ�������V(CO)��
����ʣ����������Ϊa L����ԭ�������V(CO) : V(H2)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������˵������ȷ�� �� ��
�ٳ����£�21 g C3H6��C4H8�Ļ�����к��е�̼ԭ����Ϊ1.5 NA
�� 14.2 g �����ƹ����к���0.1NA�������Ʒ��ӣ�
�۳��³�ѹ�£�11.2 L���������ķ�����Ϊ0.5 NA��
��10ml 18 mol/L��Ũ������������þ��Ӧʱת�Ƶĵ�����Ϊ 0.18 NA
�ݱ�״���£���H2O2�ֽ��Ƶ�4.48LO2ת�Ƶĵ�����ĿΪ0.4NA
��2��D216O�к��е�������������������������ΪNA
A���٢ڢ� B���ۢ� C���ܢݢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��[ͬ��]2015���ʱ����³�ư����2����ʱ6Ԫ�����ڱ���Ԫ�������ɣ������棩 ���ͣ�ѡ����
����λ��KOH��Mg(OH)2֮�������������( )
A��RbOH B��Al(OH)3
C��LiOH D��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��[ͬ��]2015��ͬ����ʱ���˽�ѡ��5��2-1Ȳ�� ֬������Դ����Ӧ�ã������棩 ���ͣ�ѡ����
��ȲΪԭ����ȡCHClBr��CH2Br�����з������ȡ����( )
A������HBr�ӳɺ�����HCl�ӳ�
B������HCl�ӳɺ�����Br2�ӳ�
C������H2��ȫ�ӳɺ�����Cl2��Br2ȡ��
D������Cl2�ӳɺ�����HBr�ӳ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com