
【题目】铜是生活中常见的金属,请回答下列问题:
(1)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快变蓝色,试写出该反应的离子方程式__________________________。
(2)将硫酸铜溶液和碳酸钠溶液混合,会析出Cu2(OH)2CO3绿色固体,试写出该反应的离子方程式_________________________________。
(3)火法炼铜的原理:Cu2S+O2![]() 2Cu+SO2,在该反应中每生成1 mol Cu,转移________ mol e-。
2Cu+SO2,在该反应中每生成1 mol Cu,转移________ mol e-。
(4)据报道,有一种细菌在有氧气存在的酸性溶液中,可将黄铜矿CuFeS2氧化成硫酸盐:4CuFeS2+2H2SO4+17O2===4CuSO4+2Fe2(SO4)3+2H2O。利用反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):

①检验溶液B中Fe3+是否被除尽的实验方法_____________________。
②在实验室中,设计方案,从溶液B中提炼金属铜(要求:方案只用一个反应来完成)。写出方案中的化学方程式:___________________________。
③从溶液B中获取胆矾的操作b是___________,____________,过滤,洗涤,干燥。
【答案】 Cu+H2O2+2H+=Cu2++2H2O 2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑ 3 取样,加KSCN,若变红则含Fe3+,未被除尽;若不变红,则除尽 CuSO4+Fe=Cu+FeSO4 蒸发浓缩 冷却结晶
【解析】考查化学工艺流程,(1)滴入H2O2溶液后,溶液很快变蓝色,说明Cu→Cu2+,H2O2作氧化剂,离子反应方程式为Cu+H2O2+2H+=Cu2++2H2O;(2)生成Cu2(OH)2CO3,部分Cu2+与CO32-发生双水解反应,产生CO2,其离子反应方程式为:2Cu2++2CO32-+H2O=Cu2(OH)2CO3↓+CO2↑;(3)根据反应方程式,Cu2S中Cu的价态由+1→0价,化合价降低,S的价态由-2价→+4价,化合价升高,O的价态由0价→-2价,化合价降低,计算转移电子物质的量,可以通过S进行计算,生成1molCu,则消耗0.5molCu2S,即转移电子物质的量为0.5×6mol=3mol;(4)①检验是否Fe3+被除尽,一般用KSCN检验,如果溶液变红,说明含有Fe3+,否则不含有,操作是:取样,加KSCN,若变红则含Fe3+,未被除尽;若不变红,则除尽;②根据流程,溶液B中含有Cu2+,制备Cu,需要加入Fe,发生Fe+Cu2+=Cu+Fe2+;③得到胆矾,胆矾中含有结晶水,采用的是蒸发浓缩、冷却结晶、过滤、干燥的方法。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】对于反应中的能量变化,表述正确的是:
A. 氧化反应均为吸热反应
B. 断开化学键的过程会放出能量
C. 加热才能发生的反应一定是吸热反应
D. 放热反应中,反应物的总能量大于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1mol的硫蒸汽和硫固体分别完全燃烧,前者△H比后者小
B. 在101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热
C. 由C(s,石墨)═C(s,金刚石);△H=+1.9kJmol-1 可知,金刚石比石墨稳定
D. 反应热就是反应中放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
请回答该实验中的问题.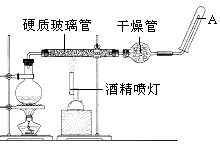
(1)写出该反应的反应方程式:
(2)如何检验该装置的气密性
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 .
(4)酒精灯和酒精喷灯点燃的顺序是 , 为什么
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下反应最符合绿色化学原子经济性要求的是( )
A. 用SiO2制备高纯硅 B. 乙烯聚合为聚乙烯高分子材料
C. 工业煅烧石灰石制CaO D. 以铜和浓硝酸为原料生产硝酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔
B. 碘盐中的碘可以直接用淀粉检验
C. 硫酸氢钠属于盐类,其水溶液显中性
D. 碳酸氢钠可以用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍,X、Y的核电荷数之比为3:4。W-的最外层为8电子结构。金属单质Z在空气中燃烧生成的化合物可与水发生氧化还原反应。下列说法正确的是
A. 元素Y、Z的简单离子的电子层结构不同
B. 原子半径大小:r(X)<r(Y),r(Z)>r(W)
C. 化合物Z2Y和Z2XY3中都只存在离子键
D. 常温下,W的单质与Z的最高价氧化物水化物的溶液反应生成两种盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com