
| A. | OH- | B. | Na+ | C. | HCO3- | D. | Cl- |
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=$\sqrt{Kw}$的溶液 | B. | pH=7 的溶液 | ||
| C. | c(H+)=10-14的溶液 | D. | 加酚酞显无色的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
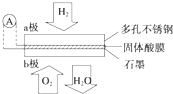 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构如图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )| A. | b极上的电极反应式为:O2+2H2O+4e-═4OH- | |
| B. | H+由a极通过固体酸电解质传递到b极 | |
| C. | 每转移0.1 mol电子,消耗1.12 L的H2 | |
| D. | 电子通过外电路从b极流向a极 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 发生水解反应时,被破坏的键是①和③ | |
| B. | 发生消去反应时,被破坏的键是①和③ | |
| C. | 发生水解反应时,被破坏的键是① | |
| D. | 发生消去反应时,被破坏的键是①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高铁酸钾的还原产物易水解形成胶体,可使水中悬浮物凝聚沉降 | |
| B. | 工业上制备高铁酸钠时每生成1mol还原产物,转移3mol电子 | |
| C. | 高铁酸钾中Fe为+6价,具有强氧化性,能消毒杀菌 | |
| D. | 高铁酸钾能除去水中溶解的H2S等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | 仅④⑤ | C. | 仅①②③ | D. | 除⑤⑦外 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某个多电子原子的3p能级上仅有两个电子,它们的自旋状态必然相反 | |
| B. | 在一个多电子原子中,不可能有两个运动状态完全相同的电子 | |
| C. | 在一个多电子原子中,不可能有两个能量相同的电子 | |
| D. | 在一个多电子原子中,N层上的电子能量肯定比M层上的电子能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
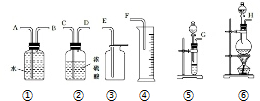 现有一定量的乙醚和乙醇的混合物试样.请从图中选用适当的实验装置,设计一个最简单的实验,测定试样中乙醇的含量.可供选用的反应物和试剂为:新制的生石灰、浓硫酸、蒸馏水、金属钠、碱石灰、无水硫酸铜.
现有一定量的乙醚和乙醇的混合物试样.请从图中选用适当的实验装置,设计一个最简单的实验,测定试样中乙醇的含量.可供选用的反应物和试剂为:新制的生石灰、浓硫酸、蒸馏水、金属钠、碱石灰、无水硫酸铜.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com