
| A、CuCl2=Cu+Cl2↑ |
| B、Na2CO3=2Na++CO32- |
| C、H2SO4=2H++S6++4O2- |
| D、Ba(OH)2=Ba+2OH |


 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
| A、直径介于1nm~100nm之间的微粒称为胶体 |
| B、电泳现象可证明胶体带电荷 |
| C、利用丁达尔效应可以区别溶液与胶体 |
| D、按照分散质和分散剂状态不同(固、液、气),它们之间可有6种组合方式 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B、常温常压下,NO2和N2O4的混合物46g中约含有2NA个氧原子 |
| C、Na2O2与H2O反应生成1.12L O2(标准状况),反应中转移的电子数为6.02×1022 |
| D、标准状况下,80g SO3中含3NA个氧原子,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,28 g N2所含的分子数多于NA |
| B、标况下,16 g O2所含原子数是NA |
| C、电子数是NA的NH3的物质的量是1 mol |
| D、17 g OH-中质子总数比电子总数多NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| B、碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| C、盛装氢氧化钠溶液的试剂瓶不可以用玻璃塞:SiO2+2Na++2 OH-=Na2SiO3+H2O |
| D、向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能跟强碱溶液反应的氧化物就是酸性氧化物 |
| B、酸性氧化物都可以与水反应可生成酸 |
| C、金属氧化物不一定是碱性氧化物 |
| D、不能跟酸反应的氧化物一定能和碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
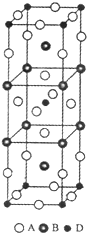 前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子总数相差为8;与B位于同一周期的C和D,它们的价电子层排布中未成对电子数分别为4和2,且原子序数相差为2.
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子总数相差为8;与B位于同一周期的C和D,它们的价电子层排布中未成对电子数分别为4和2,且原子序数相差为2.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com