
某可逆反应平衡常数表达式为K= 。达到平衡状态时,如果升高温度(其他条件不变),则c(NO)减小。下列说法正确的是
。达到平衡状态时,如果升高温度(其他条件不变),则c(NO)减小。下列说法正确的是
( )
A.反应的热化学方程式为NO2(g)+SO2(g)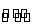 NO(g)+SO3(g) ΔH>0
NO(g)+SO3(g) ΔH>0
B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深
C.混合气体的平均摩尔质量保持不变,说明反应已达平衡
D.使用合适的催化剂可使该反应的反应速率和平衡常数增大
科目:高中化学 来源: 题型:
中学化学中很多“规律”都有适用范围,下列根据有关规律推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO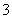 )=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是 ( )
)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是 ( )
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量水能使溶液恢复到电解前的浓度的是( )
A.AgNO3 B.Na2SO4
C.CuCl2 D.HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为相互串联的甲、乙两个电解池,X、Y为直流电源的两个电极。电解过程中,发现石墨电极附近先变红。请回答:
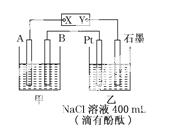
(1)电源X极为______极(填“正”或“负”),乙池中Pt电极上的电极反应式为______。
(2)甲池若为电解精炼铜的装置,其阴极增重12.8 g,则乙池中阴极上放出的气体在标准状况下的体积为______,电路中通过的电子为______mol。
(3)若乙池剩余溶液的体积仍为400 mL,则电解后所得溶液c(OH-)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)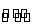 B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如下图所示。回答下列问题:
B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如下图所示。回答下列问题:
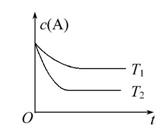
(1)上述反应的温度T1________T2,平衡常数K(T1)________K(T2)。(填“大于”“小于”或“等于”)
(2)若温度T2时,5 min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为________。
②反应的平衡常数K=________。
③反应在0~5 min区间的平均反应速率v(A)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
2.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g) PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
A.小于0.40 mol B.大于0.80 mol
C.等于0.80 mol D.大于0.40 mol,小于0.80 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com