

·ÖĪö ĀĮĶĮæóÖŠ¼ÓĮņĖįČܽāŃõ»ÆĀĮÉś³ÉĮņĖįĀĮŗĶĖ®£¬Ąė×Ó·½³ĢŹ½£ŗAl2O3+6H+=2Al3++3H2O£»Fe2O3ÓėĮņĖį·“Ӧɜ³ÉĢśĄė×Ó£¬Al2O3ÓėĮņĖį·“Ӧɜ³ÉĀĮĄė×Ó£¬¶ųSiO2²»ÓėĮņĖį·¢Éś·“Ó¦£¬¹żĀĖŗóµÄĀĖŌüĪŖSiO2£»ČÜŅŗÖŠŗ¬ÓŠAl3+”¢Fe3+ŅņĪŖÉŁĮæµÄFe2O3¹ŹÉś³ÉµÄFe3+Ņ²ŹĒÉŁĮæµÄ£¬¶ų²śĪļÖŠn£ØAl3+£©©sn£ØFe3+£©=1£ŗ1£¬ĖłŅŌŅŖ½ųŠŠŌöĢś£¬¼ÓČėµÄFeSO4±»Ė«ŃõĖ®ŌŚĖįŠŌČÜŅŗÖŠŃõ»ÆÉś³ÉFe3£¬H2O2+2Fe2++2H+=2H2O+2Fe3+ĒāŃõ»Æøʶ¼æÉŅŌµ÷½ŚpHÉś³ÉµÄĮņĖįøĘČܽā¶Č½ĻŠ”£¬Ź¹Éś³ÉĪļÖŠŌÓÖŹ½ĻÉŁ£¬¹żĀĖ³żČ„ĮņĖįøĘ£¬¼ÓČėĪČ¶Ø¼ĮæÉŅŌµĆµ½²śĪļ£®
£Ø1£©ĪŖĮĖĖį½ž³ä·Ö£¬³żĮĖ¼ÓČČ»¹æÉŅŌĶعż½Į°č¼ÓČėČܽā£»
£Ø2£©ĮņĖįČܽāŃõ»ÆĀĮÉś³ÉĮņĖįĀĮŗĶĖ®£¬Ąė×Ó·½³ĢŹ½£ŗAl2O3+6H+=2Al3++3H2O£»£Ø2£©Fe2O3ÓėĮņĖį·“Ӧɜ³ÉĢśĄė×Ó£¬Al2O3ÓėĮņĖį·“Ӧɜ³ÉĀĮĄė×Ó£¬¶ųSiO2²»ÓėĮņĖį·¢Éś·“Ó¦£¬¹Ź¹żĀĖŗóµÄĀĖŌüĪŖSiO2£»£Ø3£©¼īŹ½ĮņĖįĀĮĢśÖŠĀĮĢśµÄĻµŹżĻąĶ¬ĘäĪļÖŹµÄĮæ±ČŅ²Ó¦ĻąµČ£¬¹Źn£ØAl3+£©©sn£ØFe3+£©=1£ŗ1£»
£Ø4£©ĒāŃõ»ÆÄĘŗĶĒāŃõ»Æøʶ¼æÉŅŌµ÷½ŚpH£¬µ«ĒāŃõ»ÆÄĘ·“Ӧɜ³ÉµÄĮņĖįÄĘČÜŅŗĖ®£¬ÓėÉś³ÉĪļ¼īŹ½ĮņĖįĀĮĢś»ģŗĻŌŚČÜŅŗÖŠ²»Ņ×·ÖĄė£¬¶ųĮņĖįøĘČܽā¶Č½ĻŠ”£¬Ź¹Éś³ÉĪļÖŠŌÓÖŹ½ĻÉŁ£»
£Ø5£©Éś³É¾ŪŗĻĮņĖįĀĮĢśµÄ·“Ó¦Al3++Fe3++mSO42-+nH2O$\frac{\underline{\;ĪČ¶Ø¼Į\;}}{”÷}$ AlFe£ØOH£©n£ØSO4£©m+nH+£»
£Ø6£©ĢśŃĪĪŖÖ÷£¬Fe3+Ęš¾»Ė®×÷ÓĆŹĒŅņĪŖFe3+Ė®½āæÉŅŌÉś³ÉFe£ØOH£©3½ŗĢ壮
½ā“š ½ā£ŗ£Ø1£©ĪŖĮĖĖį½ž³ä·Ö£¬³żĮĖ¼ÓČČ»¹æÉŅŌĶعż½Į°č¼ÓĖŁČܽā£¬¹Ź“š°øĪŖ£ŗ½Į°č£»
£Ø2£©ĮņĖįČܽāŃõ»ÆĀĮÉś³ÉĮņĖįĀĮŗĶĖ®£¬Ąė×Ó·½³ĢŹ½£ŗAl2O3+6H+=2Al3++3H2O£»£Ø2£©Fe2O3ÓėĮņĖį·“Ӧɜ³ÉĢśĄė×Ó£¬Al2O3ÓėĮņĖį·“Ӧɜ³ÉĀĮĄė×Ó£¬¶ųSiO2²»ÓėĮņĖį·¢Éś·“Ó¦£¬¹Ź¹żĀĖŗóµÄĀĖŌüĪŖSiO2£¬¹Ź“š°øĪŖ£ŗSiO2£»
£Ø3£©¼īŹ½ĮņĖįĀĮĢśÖŠĀĮĢśµÄĻµŹżĻąĶ¬ĘäĪļÖŹµÄĮæ±ČŅ²Ó¦ĻąµČ£¬¹Źn£ØAl3+£©©sn£ØFe3+£©=1£ŗ1£¬¹Ź“š°øĪŖ£ŗ1£ŗ1£»
£Ø4£©ĒāŃõ»ÆÄĘŗĶĒāŃõ»Æøʶ¼æÉŅŌµ÷½ŚpH£¬µ«ĒāŃõ»ÆÄĘ·“Ӧɜ³ÉµÄĮņĖįÄĘČÜŅŗĖ®£¬ÓėÉś³ÉĪļ¼īŹ½ĮņĖįĀĮĢś»ģŗĻŌŚČÜŅŗÖŠ²»Ņ×·ÖĄė£¬¶ųĮņĖįøĘČܽā¶Č½ĻŠ”£¬Ź¹Éś³ÉĪļÖŠŌÓÖŹ½ĻÉŁ£¬¹Ź“š°øĪŖ£ŗÓĆCa£ØOH£©2µ÷pHÄܵƵ½Čܽā¶Č½ĻŠ”µÄCaSO4£¬µĆµ½µÄ²śĘ·½Ļ“棻
£Ø5£©øł¾ŻÉś³ÉĪļµÄ·Ö×Ó×é³É£¬Éś³É¾ŪŗĻĮņĖįĀĮĢśµÄ·“Ó¦Al3++Fe3++mSO42-+nH2O$\frac{\underline{\;ĪČ¶Ø¼Į\;}}{”÷}$ AlFe£ØOH£©n£ØSO4£©m+nH+£¬
¹Ź“š°øĪŖ£ŗAl3++Fe3++mSO42-+nH2O$\frac{\underline{\;ĪČ¶Ø¼Į\;}}{”÷}$ AlFe£ØOH£©n£ØSO4£©m+nH+£»
£Ø6£©ĢśŃĪĪŖÖ÷£¬Fe3+Ęš¾»Ė®×÷ÓĆŹĒŅņĪŖFe3+Ė®½āæÉŅŌÉś³ÉFe£ØOH£©3½ŗĢ壬Fe£ØOH£©3½ŗĢå¾ßÓŠĪüø½ŠŌæÉŅŌÓĆÓŚ¾»Ė®£¬¹Ź“š°øĪŖ£ŗFe£ØOH£©3£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄė”¢Ģį“æÖŖŹ¶£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦µÄ漲飬עŅā°ŃĪÕŹµŃéµÄŌĄķŗĶ²Ł×÷·½·Ø£¬ĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø
Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā

| A£® | a¼«ŹĒÖ±Į÷µēŌ“µÄÕż¼« | |
| B£® | Fe¼«ŹĒŃō¼« | |
| C£® | Pt¼«²śÉśµÄĘųĢåĢå»żŹĒAg¼«²śÉśĘųĢåĢå»żµÄ2±¶ | |
| D£® | ĮņĖįĶČÜŅŗµÄÅØ¶Č²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹čŹĒ¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖ³É·Ö | |
| B£® | Ēā·śĖį¾ßÓŠĒæĖįŠŌ£¬æÉÓĆÓŚŹ“æĢ²£Į§ | |
| C£® | Ģ¼ĻĖĪ¬ŹĒŅ»ÖÖŠĀŠĶÓŠ»śøß·Ö×Ó²ÄĮĻ | |
| D£® | ¹č½ŗæÉ×öŅ©Ę·ŗĶŹ³Ę·µÄøÉŌļ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŃŠ¾æNO2”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮
ŃŠ¾æNO2”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢Ba2+”¢Br-”¢CO32- | B£® | Fe3+”¢Na+”¢NO3-”¢SCN- | ||
| C£® | Al3+”¢NO3-”¢I-”¢SO42- | D£® | Al3+”¢Cl-”¢SO42-”¢HCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
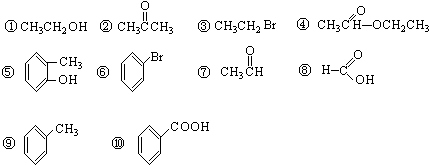
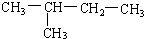 £Ø8£©
£Ø8£©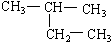 £Ø9£©CH2=CH-CH3 £Ø10£©
£Ø9£©CH2=CH-CH3 £Ø10£©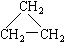
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņŃĪĖįÖŠ¼ÓČė¼øµĪĢ¼ĖįÄĘČÜŅŗ£ŗH++CO32-ØTHCO3- | |
| B£® | ĻņČżĀČ»ÆĢśČÜŅŗÖŠ¼ÓČėµā»Æ¼ŲČÜŅŗ£ŗFe3++2I-ØTFe2++I2 | |
| C£® | ¹żĮæµÄĢś·Ū¼ÓČėĻ”ĻõĖįÖŠ£ŗFe+4H++NO3-ØTFe3++NO”ü+2H2O | |
| D£® | µČĪļÖŹµÄĮæÅØ¶ČµÄĆ÷·ÆČÜŅŗÓėĒāŃõ»Æ±µČÜŅŗ°“Ģå»ż±Č1£ŗ2»ģŗĻ£ŗAl3++2SO42-+2Ba2++4OH-ØTAlO2-+2BaSO4”ż+2H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com