
| A. | $\frac{4x-2y}{a}$ | B. | $\frac{2x-y}{a}$ | C. | $\frac{8x-3y}{2a}$ | D. | $\frac{8x-3y}{a}$ |
分析 根据反应Ba2++SO42-=BaSO4↓可知硫酸铝钾和硫酸钾中硫酸根离子的总物质的量,根据反应Al3++4OH-=AlO2-+2H2O可知铝离子的物质的量,从而可知硫酸铝钾中硫酸根离子的物质的量,然后计算出硫酸钾的物质的量,根据硫酸钾的化学式可计算出钾离子的物质的量,再根据c=$\frac{n}{V}$计算出原混合溶液中的c(K+).
解答 解:SO42-离子完全沉淀的反应为:Ba2++SO42-=BaSO4↓,消耗了xmolBaCl2,则每份混合液中含有SO42-的总物质的量为xmol,
另一份滴加KOH溶液,使Al3+离子先沉淀后又恰好溶解,反应的总离子方程式为:Al3++4OH-=AlO2-+2H2O,消耗了ymol KOH,则每份溶液中含有KAl(SO4)2的物质的量为ymol×$\frac{1}{4}$=0.25ymol,每份溶液中KAl(SO4)2含有硫酸根离子的物质的量为:0.25ymol×2=0.5ymol,
所以每份溶液中含有K2SO4的物质的量为:xmol-0.5ymol=(x-0.5y)mol,每份溶液中含有钾离子的物质的量为:(x-0.5y)mol×2=(2x-y)mol,
所以原混合溶液中的钾离子的浓度为:c(K+)=$\frac{(2x-y)mol}{\frac{a}{2}L}$=$\frac{4x-2y}{a}$mol/L,
故选A.
点评 本题考查混合物的有关计算、物质的量浓度的计算等,题目难度中等,明确发生的离子反应及溶液不显电性是解答本题的关键,注意熟悉物质的量浓度的计算公式.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Mg2+、SO42-、Cl- | B. | Fe3+、K+、Cl-、NO3- | ||
| C. | K+、Ba2+、NO3-、SO42- | D. | Na+、NH4+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 产生${\;}_{30}^{65}$Zn的反应是聚变反应 | |
| B. | ${\;}_{30}^{64}$Zn和${\;}_{30}^{65}$Zn具有相同的质子数 | |
| C. | ${\;}_{30}^{65}$Zn衰变放射出γ射线时,发生质量亏损,质量亏损并不意味着质量被消灭 | |
| D. | γ射线在真空中传播的速度是3.0×108m/s | |
| E. | γ射线是由于锌原子的内层电子激发产生的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
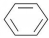 +HNO3(浓)$\frac{\underline{\;\;\;浓硫酸\;\;\;}}{50~60℃}$
+HNO3(浓)$\frac{\underline{\;\;\;浓硫酸\;\;\;}}{50~60℃}$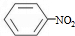 +H2O设计一个实验制取一定量的纯净硝基苯.有关信息见下表:
+H2O设计一个实验制取一定量的纯净硝基苯.有关信息见下表:| 物质 | 熔点/℃ | 沸点/℃ | 相对密度/(20℃) | 毒性 | 水溶性 |
| 苯 | 5.5 | 80.1 | 0.8794 | 有 | 不溶于水 |
| 硝酸 | -41.59 | 83 | 1.503 | - | 易溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 有 | 不溶于水 |
| 硫酸 | 10.0 | 338 | 1.84 | - | 易溶于水 |

| 1 | 用蒸馏水洗涤反应混合液,分液后取下层液体 |
| 2 | |
| 3 | |
| 4 | |
| 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
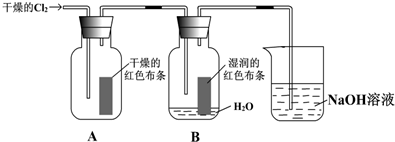
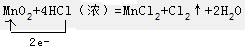
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入NaOH溶液,生成灰白色沉淀迅速变成灰绿色,最后变成红褐色 | |
| B. | 加入NaOH溶液,生成红褐色沉淀 | |
| C. | 加入硫氰化钾溶液,显示红色 | |
| D. | 加入氨水,生成红褐色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com