
����Ŀ�������������в����ķ�ˮ�������ǻ�����Ⱦ����ҪԴͷ���ڻ��������������ǿ�����I2O5��Na2SO3�Ȼ�����Ʒʵ�ֶԷ�ˮ�ͷ�����������
��1������I2O5�������Դ�������H2S���õ�S��I2���ֵ��ʣ�������Ӧ�Ļ�ѧ����ʽΪ________________��
��2������I2O5Ҳ������CO����Ⱦ���䷴Ӧԭ��ΪI2O5(s)+5CO(g)![]() 5CO2(g)+I2(s) ��H����֪�ڲ�ͬ�¶ȣ�T1��T2���£���װ������I2O5�����2 L�����ܱ�������ͨ��2 mol CO�����CO2��������������(CO2)��ʱ��t�ı仯������ͼ��ʾ��
5CO2(g)+I2(s) ��H����֪�ڲ�ͬ�¶ȣ�T1��T2���£���װ������I2O5�����2 L�����ܱ�������ͨ��2 mol CO�����CO2��������������(CO2)��ʱ��t�ı仯������ͼ��ʾ��
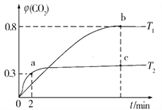
���¶�ΪT2ʱ��0��2 min �ڣ�CO2��ƽ����Ӧ���� ��(CO2)=______________��
��b��ʱCO��ת����Ϊ_______����ѧ��Ӧ��ƽ�ⳣ��K=_____�������ʽ����
�۷�Ӧ��I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)����H______0������>����<������=������
5CO2(g)+I2(s)����H______0������>����<������=������
��������Ӧ��T1�´ﵽƽ��ʱ�����������г������ʵ�����Ϊ2 mol��CO��CO2���壬��ѧƽ��________������������ �������������������ƶ���
�����������Ա�ʾ������Ӧ�ﵽƽ��״̬����____________������ĸ����
A�������ڵ�ѹǿ���ٱ仯 B���������ƽ����Է����������ٱ仯
C����������ܶȲ��ٱ仯 D����λʱ��������CO������CO2�����ʵ���֮��Ϊ1��1
��3��Na2SO3���л�ԭ�ԣ���ˮ��Һ��������Cl2(g)�����ٻ�����Ⱦ��
��֪��Ӧ��
��Na2SO3(aq)+Cl2(g)+H2O(l) ![]() Na2SO4(aq)+2HCl(aq) ��H1=a kJ��mol1
Na2SO4(aq)+2HCl(aq) ��H1=a kJ��mol1
��Cl2(g)+H2O(l) ![]() HCl(aq)+HClO(aq) ��H2=b kJ��mol1
HCl(aq)+HClO(aq) ��H2=b kJ��mol1
��д��Na2SO3(aq)��HClO(aq)��Ӧ���Ȼ�ѧ����ʽ��________________________��
���𰸡� I2O5 + 5 H2S = 5S + I2 + 5H2O 0.15 mol��L-1 ��min-1 80% C5(CO2)/ C5(CO) < ���� BC Na2SO3(aq) + HClO(aq) ![]() Na2SO4(aq) + 2HCl(aq) ��H=��a-b��kJ��mol1
Na2SO4(aq) + 2HCl(aq) ��H=��a-b��kJ��mol1
����������1������I2O5�������Դ�������H2S��H2S������ΪS��I2O5����ԭΪI2�����ݻ��ϼ�������������Լ������غ㶨�ɣ�����д���÷�Ӧ�Ļ�ѧ����ʽΪI2O5 + 5 H2S = 5S + I2 + 5H2O��
��2���÷�Ӧ��һ��������������ֲ���ķ�Ӧ�����Է�Ӧǰ����������ʵ������ֲ��䡣��ͼ���֪����Ӧ��T2ʱ�ȴﵽƽ��״̬������T1<T2���¶�T1�����ߵ�T2����(CO2)��С��˵������Ӧ�Ƿ��ȷ�Ӧ��
���¶�ΪT2ʱ��0��2 min �ڣ���(CO2)��0���ߵ�0.3����CO2�ı仯��Ϊ2mol![]() ��CO2��ƽ����Ӧ������(CO2)=
��CO2��ƽ����Ӧ������(CO2)= ![]() 0.15 mol��L-1 ��min-1��
0.15 mol��L-1 ��min-1��
��b��ʱ��(CO2)=0.8��CO�ı仯��Ϊ0.8![]() ��CO��ת����Ϊ
��CO��ת����Ϊ![]() 80% ������������͵ⶼ�ǹ��壬���Ըû�ѧ��Ӧ��ƽ�ⳣ��K= C5(CO2)/ C5(CO)��
80% ������������͵ⶼ�ǹ��壬���Ըû�ѧ��Ӧ��ƽ�ⳣ��K= C5(CO2)/ C5(CO)��
�۷�Ӧ��I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)����H<0��
5CO2(g)+I2(s)����H<0��
��������Ӧ��T1�´ﵽƽ��ʱ��c(CO)=0.2mol/L��c(CO2)=0.8mol/L��K= C5(CO2)/ C5(CO)= ![]() �����������г������ʵ�����Ϊ2 mol��CO��CO2���壬Qc=
�����������г������ʵ�����Ϊ2 mol��CO��CO2���壬Qc=![]() <K����ѧƽ�������ƶ���
<K����ѧƽ�������ƶ���
����Ϊ��Ӧǰ��������������䣬���������ڵ�ѹǿ�������仯��CO��CO2�Ļ�ѧ����������ͬ�ģ����Ե�λʱ��������CO������CO2�����ʵ���֮��ʼ��Ϊ1��1��ʼ�ղ�������ݲ�����Ϊƽ��״̬�ı�־���������ƽ����Է��������ͻ�������ܶ��DZ��������Կ��Ա�ʾ������Ӧ�ﵽƽ��״̬���ǻ������ƽ����Է����������ٱ仯�ͻ�������ܶȲ��ٱ仯����BC��
��3����Na2SO3(aq)+Cl2(g)+H2O(l) ![]() Na2SO4(aq)+2HCl(aq) ��H1=a kJ��mol1����Cl2(g)+H2O(l)
Na2SO4(aq)+2HCl(aq) ��H1=a kJ��mol1����Cl2(g)+H2O(l) ![]() HCl(aq)+HClO(aq) ��H2=b kJ��mol1������-�ڵ���Na2SO3(aq) + HClO(aq)
HCl(aq)+HClO(aq) ��H2=b kJ��mol1������-�ڵ���Na2SO3(aq) + HClO(aq) ![]() Na2SO4(aq)+ 2HCl(aq)��������H=��a-b��kJ��mol1����Na2SO3(aq)��HClO(aq)��Ӧ���Ȼ�ѧ����ʽΪNa2SO3(aq) + HClO(aq)
Na2SO4(aq)+ 2HCl(aq)��������H=��a-b��kJ��mol1����Na2SO3(aq)��HClO(aq)��Ӧ���Ȼ�ѧ����ʽΪNa2SO3(aq) + HClO(aq) ![]() Na2SO4(aq) + 2HCl(aq) ��H=��a-b��kJ��mol1��
Na2SO4(aq) + 2HCl(aq) ��H=��a-b��kJ��mol1��


 ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д� С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�ش����⣺ 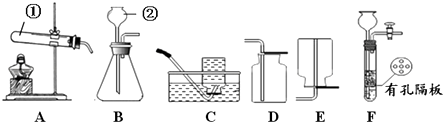
��1��д���б�ŵ��������ƣ��� �� �� ��
��2��ʵ�����ø��������ȡO2�Ļ�ѧ����ʽΪ �� ��A��Cװ����ȡO2ʱ��Ϊ��ֹ������ؽ��뵼�ܣ��ɲ�ȡ�Ĵ�ʩ�� ��
��3��ʵ������B��Dװ����ȡCO2�Ļ�ѧ����ʽΪ �� ��������װ����B��ΪF�����ŵ��� ��
��4��SO2����ɫ�д̼�����ζ���ж����壬�ܶȱȿ�����������ˮ��SO2��ijЩ��ѧ������CO2���ƣ�ʵ���г���NaOH��Һ����SO2β��������ͼ��ʾװ���ռ�һƿ�����SO2 �� װ���е��ܰ�������������˳�������ݣ�����ţ���ͼ��©�������������ձ���NaOH��Һ�����������û�ѧ����ʽ��ʾ���� 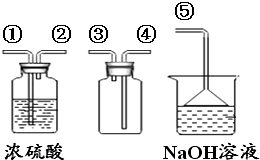
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е������ܹ�����������ͬһ��Һ�е��� (����)
A. CO32-��Ba2����Na����NO3- B. H����Al3����OH����SO42-
C. OH����NO3-��K����Na�� D. K����Fe3����Cl����OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£�H2��g�� + CO2��g�� ![]() H2O��g��+ CO��g����ƽ�ⳣ��K=9/4�����¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��g���� CO2��g��������ʼŨ�����±���ʾ
H2O��g��+ CO��g����ƽ�ⳣ��K=9/4�����¶��£��ڼס��ҡ������������ܱ������У�Ͷ��H2��g���� CO2��g��������ʼŨ�����±���ʾ
��ʼŨ�� | �� | �� | �� |
C��H2��/ mol��l-1 | 0.010 | 0.020 | 0.020 |
C��CO2��/ mol��l-1 | 0.010 | 0.010 | 0.020 |
�����жϲ���ȷ����
A. ƽ��ʱ������CO2 ��ת���ʴ���60%
B. ƽ��ʱ���ͱ���H2 ��ת���ʾ���60%
C. ƽ��ʱ������C��CO2���Ǽ��е�2������0.012 mol��l-1
D. ��Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£�m g����A��n g����B�ķ�����Ŀһ���࣬����˵������ȷ������ ��
A. �����������£������ַ��ӱ���ԭ��ɣ�������Է�������֮��Ϊm��n
B. 25 ����1.25��105 Paʱ����������ܶ�֮��Ϊn��m
C. ͬ������A��B�ڷDZ�״���£��������֮��Ϊn��m
D. ��ͬ״���£�ͬ���������A��B������֮��Ϊm��n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������һƿ��84����Һ������װ˵�����£������������Ϣ�����֪ʶ�жϣ����з�������ȷ������ ��

A. ����84����Һ�������ʵ���Ũ��ԼΪ4.0 mol��L��1
B. һƿ����84����Һ�����ڷ���һ��ʱ���Ũ�Ȼ��С
C. ȡ100 mL����84����Һ��ϡ��100������������ϡ�ͺ���Һ��c(Na��)ԼΪ0.04mol��L��1
D. ���ĸ���84����Һ�����䷽������NaClO�������ƺ�25%NaClO������Һ480 mL����Ҫ������NaClO��������Ϊ143 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С����ʵ����̽�����������(NH2COONH4)�ֽⷴӦƽ�ⳣ����ˮ�ⷴӦ���ʵIJⶨ����һ���������İ�������粒����������Ƶ��ܱ����������(��������������䣬��������������Բ���)���ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4(s)![]() 2NH3(g)��CO2(g)
2NH3(g)��CO2(g)
ʵ���ò�ͬ�¶��µ�ƽ�����������±���

��1�������жϸ÷ֽⷴӦ�Ѿ��ﵽƽ�����________(����ĸ���)��
A��2v(NH3)��v(CO2)
B���ܱ���������ѹǿ����
C���ܱ������л��������ܶȲ���
D���ܱ������а����������������
��2�����ݱ������ݣ���ʽ����25.0 ��ʱ�ķֽ�ƽ�ⳣ����____________________________��
��3��ȡһ�����İ�������粒������һ�����������ܱ���������У���25.0 ���´ﵽ�ֽ�ƽ�⡣���ں�����ѹ�������������������粒����������________(����������������������������)��
��4����������立ֽⷴӦ���ʱ���H____0(����>������������<������ͬ)���ر���S____0��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com