
| A、Na→NaOH→Na2CO3→NaCl |
| B、Fe→Fe(NO3)3→Fe(OH)3→Fe2O3 |
| C、Mg→MgCl2→Mg(OH)2→MgSO4 |
| D、Al→Al2O3→Al(OH)3→AlCl3 |
| 过量的硝酸 |
| 氢氧化钠 |
| 加热 |


科目:高中化学 来源: 题型:
| A、常温下将64g铜片投入过量浓硫酸中 |
| B、向100.0mL 3.00mol/L的稀硝酸中加入5.6g铁 |
| C、1mol MnO2粉末与含4mol HCl的浓盐酸共热 |
| D、常温下1mol铝片投入20.0mL 18.40mol/L硫酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中不存在任何游离态的金属单质 |
| B、金属活动性不同,冶炼方法也有所不同 |
| C、地球上金属矿物资源是有限的,因此,应提高金属矿物的利用率 |
| D、废旧金属的回收利用,有利于环境保护 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝是主族元素 |
| B、铁元素与氯气反应形成离子键 |
| C、自然界中不存在准晶体 |
| D、铜、铁都是过渡元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜比铝先获得成功冶炼原因是,铜矿较易还原,铝矿很难还原 |
| B、目前已制得的纯金属只有90多种,但制得的合金已达几千种,大量使用的不是纯金属而是它们的合金 |
| C、生铁易生锈不耐蚀,但纯铁具有耐蚀性,所以不锈钢应是最纯的铁 |
| D、废弃铝质包装既浪费金属材料又造成环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用铜做电线是由于其导电性良好 |
| B、用钨做灯丝是因为其熔点高 |
| C、铁制品表面镀铬是由于铬硬且不易被氧化 |
| D、用铝制炊具是因为铝的溶点比铁高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol铜片与含2mol H2SO4的浓硫酸共热 |
| B、1mol MnO2粉末与含2mol H2O2的溶液共热 |
| C、1mol MnO2粉末与含4mol HCl的稀溶液共热 |
| D、常温下1mol铜片投入含4mol HNO3的浓硝酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
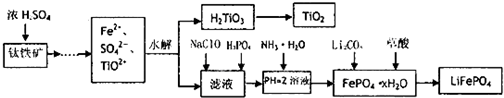
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com