
| A. | Na的含氧化合物是碱性氧化物 | |
| B. | 从海水中提取这三种元素的单质的过程都涉及氧化还原反应 | |
| C. | 这三种元素以化合态存在时形成的化学键只有离子键 | |
| D. | 加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2 |
分析 A.和酸反应生成盐和水的氧化物为碱性氧化物,反应为复分解反应;
B.氧化还原反应判断的依据是:有化合价的变化;
C.氯元素化合态存在可以形成共价键;
D.MgCl2水解生成氢氧化镁和氯化氢,加热氯化氢挥发,最终得到的固体是氢氧化镁.
解答 解:A.氧化钠为碱性氧化物,过氧化钠和酸反应发生氧化还原反应不是碱性氧化物,故A错误;
B.Na、Mg、Al为活泼金属在海水中以离子的形式存在化合价均为正值,转化成单质后,化合价变为0价,属于氧化还原反应,故B正确;
C.钠和镁化合态形成的化合物中含离子键,氯元素化合态存在形成的化合物中可以是共价键,如HCl,故C错误;
D.MgCl2水解生成氢氧化镁和氯化氢,加热氯化氢挥发,最终得到的固体是氢氧化镁,得不到氯化镁,故D错误;
故选B.
点评 本题考查了海水资源的利用、元素存在状态、氧化还原反应、盐类水解等,题目综合性强,题目难度中等,选项D为易错点,注意可水解的挥发性酸对应的盐溶液蒸干所得物质的判断.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 若生成1mol Fe,则吸收的热量小于a kJ | |
| B. | 若升高温度,正反应速率加快,逆反应速率加快,则化学平衡正向移动 | |
| C. | 若增大压强反应向正反应方向进行 | |
| D. | 若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+、NH4+、Fe3+、Ba2+ |
| 阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
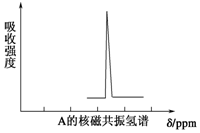 有一种新合成的高度对称的有机物A.已知10.4g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重7.2g和35.2g,经检验剩余气体为O2.
有一种新合成的高度对称的有机物A.已知10.4g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重7.2g和35.2g,经检验剩余气体为O2.
 ,其核磁共振氢谱有5个吸收峰.
,其核磁共振氢谱有5个吸收峰.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/(mol•L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醛的电子式: | B. | 乙醇分子的球棍模型: | ||
| C. |  的名称:3-甲基-2-丁烯 的名称:3-甲基-2-丁烯 | D. | CO2的分子模型示意图为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢板中的铁做负极,电极反应为Fe-2e-=Fe2+ | |
| B. | 放电时正极上有氧气生成 | |
| C. | 放电时OH-向正极移动 | |
| D. | 电池总反应为:2Li+2H2O═2LiOH+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com