
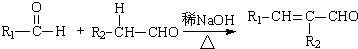 ��R��R��Ϊ�������⣩
��R��R��Ϊ�������⣩ ��R��R��Ϊ������
��R��R��������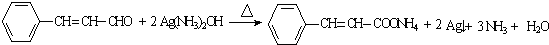 ��
��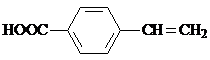 ��
�� ��
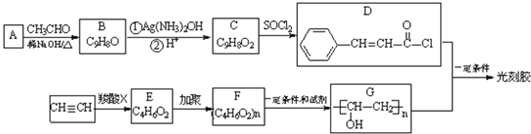
�� ���� ��D�Ľṹ��֪��A�к��б�����A��CH3CHO��Ӧ�õ�B�������ʵķ���ʽ����Ϣ����֪AΪ ��BΪ
��BΪ ��B��������Һ����������Ӧ���ữ�õ�C����CΪ
��B��������Һ����������Ӧ���ữ�õ�C����CΪ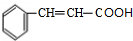 ����Ȳ������X�ӳ�����E��E�����Ӿ۷�Ӧ�õ�F����E�����к���C=C˫������Ϸ���ʽ��֪��XΪCH3COOH��E�ĺ˴Ź�������Ϊ����壬�ҷ������Ϊ3��2��1��E�ܷ���ˮ�ⷴӦ����EΪCH3COOCH=CH2��FΪ
����Ȳ������X�ӳ�����E��E�����Ӿ۷�Ӧ�õ�F����E�����к���C=C˫������Ϸ���ʽ��֪��XΪCH3COOH��E�ĺ˴Ź�������Ϊ����壬�ҷ������Ϊ3��2��1��E�ܷ���ˮ�ⷴӦ����EΪCH3COOCH=CH2��FΪ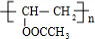 ��G��D������Ϣ��ķ�Ӧ�õ���̽������̽��Ľṹ��ʽΪ��
��G��D������Ϣ��ķ�Ӧ�õ���̽������̽��Ľṹ��ʽΪ��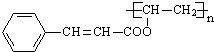 ���ݴ˽��
���ݴ˽��
��� �⣺��D�Ľṹ��֪��A�к��б�����A��CH3CHO��Ӧ�õ�B�������ʵķ���ʽ����Ϣ����֪AΪ ��BΪ
��BΪ ��B��������Һ����������Ӧ���ữ�õ�C����CΪ
��B��������Һ����������Ӧ���ữ�õ�C����CΪ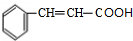 ����Ȳ������X�ӳ�����E��E�����Ӿ۷�Ӧ�õ�F����E�����к���C=C˫������Ϸ���ʽ��֪��XΪCH3COOH��E�ĺ˴Ź�������Ϊ����壬�ҷ������Ϊ3��2��1��E�ܷ���ˮ�ⷴӦ����EΪCH3COOCH=CH2��FΪ
����Ȳ������X�ӳ�����E��E�����Ӿ۷�Ӧ�õ�F����E�����к���C=C˫������Ϸ���ʽ��֪��XΪCH3COOH��E�ĺ˴Ź�������Ϊ����壬�ҷ������Ϊ3��2��1��E�ܷ���ˮ�ⷴӦ����EΪCH3COOCH=CH2��FΪ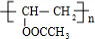 ��G��D������Ϣ��ķ�Ӧ�õ���̽������̽��Ľṹ��ʽΪ��
��G��D������Ϣ��ķ�Ӧ�õ���̽������̽��Ľṹ��ʽΪ��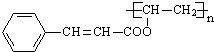 ��
��
��1��AΪ �������к�������������Ϊ��ȩ�����ʴ�Ϊ��ȩ����
�������к�������������Ϊ��ȩ�����ʴ�Ϊ��ȩ����
��2������G�Ľṹ��ʽ��֪��G�Ļ�ѧ����Ϊ����ϩ����
�ʴ�Ϊ������ϩ����
��3��FΪ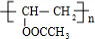 ��F����G�ķ�Ӧ����Ϊȡ����
��F����G�ķ�Ӧ����Ϊȡ����
�ʴ�Ϊ��ȡ����
��4������D�Ľṹ��ʽ��֪�������ϵ�����ԭ�ӿ��Թ��棬̼̼˫����̼��˫���ϵ�ԭ��Ҳ���Թ��棬����D��������� 18��ԭ�ӹ�ƽ�棬
�ʴ�Ϊ��18��
��5��BΪ ��B��Ag��NH3��2OH��Ӧ�Ļ�ѧ����ʽΪ
��B��Ag��NH3��2OH��Ӧ�Ļ�ѧ����ʽΪ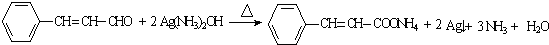 ��
��
�ʴ�Ϊ��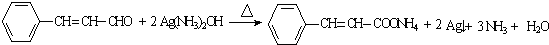 ��
��
��6����������ķ�����֪��EΪCH3COOCH=CH2��
�ʴ�Ϊ��CH3COOCH=CH2��
��7��CΪ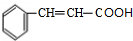 ����C������ͬ�������Һ��б�����ͬ���칹��Ϊ����������-C��COOH��=2����������-CH=CH2��-COOH�������ţ����ڼ�����֣����Թ���4�֣����б����ϵ�һ�ȴ��������ֵ�ͬ���칹��Ľṹ��ʽ��
����C������ͬ�������Һ��б�����ͬ���칹��Ϊ����������-C��COOH��=2����������-CH=CH2��-COOH�������ţ����ڼ�����֣����Թ���4�֣����б����ϵ�һ�ȴ��������ֵ�ͬ���칹��Ľṹ��ʽ��
�ʴ�Ϊ��4�� 
��8��D��G��Ӧ���ɹ�̽��Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ��������ת����ϵ�����ʵĽṹ������ʽ������������Ʒ������ƶϣ��ϺõĿ���ѧ���ķ���������������ע�����չ����ŵ�������ת�����Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ�����У�������ѹǿ�����SiCl4��ת���� | |
| B�� | ����Ӧ��ʼʱSiCl4Ϊ1 mol�����ƽ��ʱ����������ΪQ kJ | |
| C�� | ��Ӧ��4 minʱ����HClŨ��Ϊ0.12 mol/L����H2�ķ�Ӧ����Ϊ0.03 mol/��L•min�� | |
| D�� | ��Ӧ����0.025Q kJ����ʱ�����ɵ�HClͨ��100 mL 1 mol/L��NaOH��Һ��ǡ����ȫ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ������� | �������� | ��ʼ���ʵ���/mol | ƽ��ʱSO3�����ʵ���/mol | ||
| SO2 | O2 | SO3 | |||
| �� | ���º��� | 2 | 1 | 0 | 1.2 |
| �� | ���Ⱥ��� | 0 | 0 | 2 | a |
| �� | ���º�ѹ | 2 | 1 | 0 | b |
| A�� | ƽ��ʱSO3�����ʵ�����a��1.2��b��1.2 | |
| B�� | ��������ƽ�ⳣ����ͬ | |
| C�� | ���� I��SO2��ת��������������SO3��ת����֮��С��1 | |
| D�� | ����ʼʱ���������г���1.0mol SO2 ��g����0.40mol O2��g����1.40mol SO3 ��g�������ʱ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 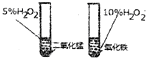 �Ƚ϶������̺�����þ�Ĵ�Ч�� | B�� | 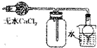 �����ռ����� | ||
| C�� | 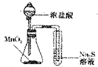 �Ƚ϶������̡���������������� | D�� |  �۲�����������ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
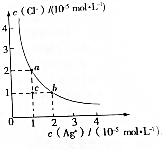
| A�� | a���b���Ӧ��Ksp��AgCl����� | |
| B�� | Ksp��AgCl��=2��10-10 | |
| C�� | �ɲ�ȡ�����ܼ��ķ���ʹ��Һ��c��䵽b�� | |
| D�� | ��֪Ksp��AgI��=8.5��10-17����KI��KCl����Һ�еμ�AgNO3��Һ����AgCl��ʼ����ʱ����Һ��$\frac{c��{I}^{-}��}{c��C{l}^{-}��}$=4.25��10-7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ̼ԭ������n�� | 6 | 8 | 10 | 12 | �� |
| �ṹ��ʽ | 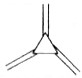 | 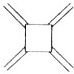 | 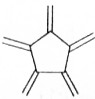 | 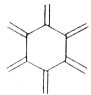 | �� |
| A�� | ��ϩ��ͨʽ�ɱ�ʾΪCnHn | |
| B�� | n=100����ϩ�����к���50��̼̼˫�� | |
| C�� | n=6����ϩ���ӵ�ͬ���칹���к�������̼̼�����Ľṹ��6�� | |
| D�� | n=8����ϩ���ӵ�ͬ���칹��������ڷ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
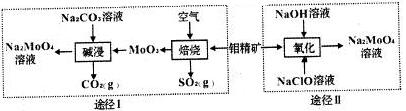
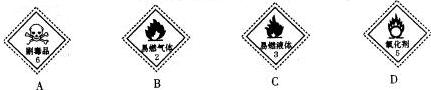
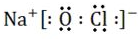 ��
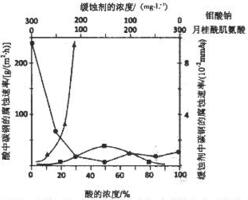
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �� H2O2
�� H2O2 NH4Cl
NH4Cl
 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com