
| A. | 46gNO2和N2O4的混合气体中含有的原子个数为3NA | |
| B. | 标准状况下,22.4L乙醇完全燃烧后生成的CO2分子数为2NA | |
| C. | 1mol苯中所含的碳碳双键数为3NA | |
| D. | 1mol Cl2与过量Fe反应,转移的电子数为3NA |
分析 A.NO2和N2O4的最简式相同为NO2,计算46g NO2中所含原子数;
B.气体摩尔体积使用对象为气体;
C.苯不是单双键交替的结构;
D.铁与氯气反应生成氯化铁,氯气不足依据氯气量计算转移电子数.
解答 解:A.NO2和N2O4的最简式相同为NO2,计算46g NO2中所含原子数=$\frac{46g}{46g/mol}$×3×NA=3NA,故A正确;
B.标准状况下乙醇不是气态,不能适用于气体摩尔体积,故B错误;
C.苯不是单双键交替的结构,故苯中不含碳碳双键,故C错误;
D.1molCl2与过量Fe反应,生成氯化铁,生成2mol氯离子,转移的电子数为2 NA,故D错误,
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件及标况下常见物质的状态,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:实验题
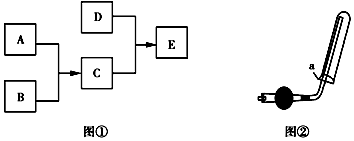
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
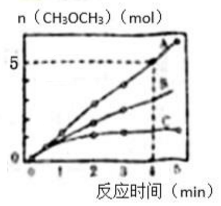 研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义.将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(1).
研究CO2转化成有机物实现碳循环对实现社会的可持续发展具有重要的意义.将燃煤废气中的CO2转化为二甲醚的反应原理为2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(1).| 序号 | 起始投料量不同的压强下, 平衡CH3OCH3(g)的量不同的压强 | P1 | P2 | P3 |
| I | 2.0molCO2 6.0molH2 | 0.10mol | 0.04mol | 0.02mol |
| II | 1.0molCO2 3.0molH2 | X1 | Y1 | Z1 |
| III | 1.0mol CH3OCH3 3.0mol H2O | X2 | Y2 | Z2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与氯气反应生成的产物仍为平面结构 | |
| B. | 甲烷可以与氯气发生反应,因此可以使氯水褪色 | |
| C. | CHCl3只有一种结构,能说明甲烷是正四面体结构 | |
| D. | 邻二氯苯只有一种结构,说明苯环不是单双键交替结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的正反应的活化能大于100kJ•mol-1 | |
| B. | 加入适当催化剂,可以改变该反应历程 | |
| C. | 一定条件下,v正(M)=2v逆(N)时,该反应达到平衡状态 | |
| D. | 断裂2分子M中的化学键吸收的能量比断裂1分子N中的化学键吸收的能量多100kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
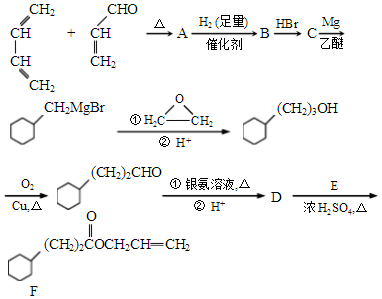
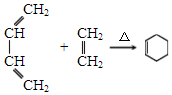
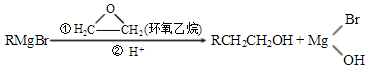
 ,A中所含官能团的名称是醛基、碳碳双键.
,A中所含官能团的名称是醛基、碳碳双键. .
.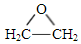 )为原料制备1丁醇,设计合成路线
)为原料制备1丁醇,设计合成路线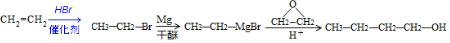 (其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)
(其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质均由原子或分子构成 | |
| B. | 已知的大部分物质属于有机物 | |
| C. | 食品加工中应严禁使用人工合成的物质 | |
| D. | 干冰、可燃冰属于同种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10% | B. | 11.1% | C. | 0.1% | D. | 20% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
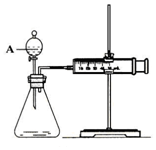 用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0,7克镁带,按图连接好装置,从A中加入20.0ml0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.记录数据如表
用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0,7克镁带,按图连接好装置,从A中加入20.0ml0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.记录数据如表| 时间/s | 0 | t | 2t | … |
| 活塞的位置/ml | 17.3 | 25.6 | 36.6 | … |
| 实验序号 | 双氧水体积/mL | 蒸馏水体积/mL | 添加的物质 |
| 1 | 10 | 0 | 4mLFeCl3 |
| 2 | 10 | 2 | 2mLCuCl2 |
 .
.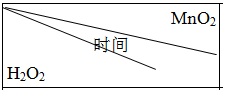 | 0.1g | 0.3g | 0.8g |
| 10mL1.5% | 223s | 67s | 36s |
| 10mL3.0% | 308s | 109s | 98s |
| 10mL4.5% | 395s | 149s | 116s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com