
国际上不提倡伊朗浓缩铀,因为铀 是制造原子弹的燃料。
是制造原子弹的燃料。 原子核内含有中子数为
原子核内含有中子数为
A.92 B.235 C.143 D.327
科目:高中化学 来源:2013-2014湖南省五市十校高一下学期期中教学质量检测化学试卷(解析版) 题型:实验题
某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了Cl元素的非金属性比Br强的实验研究。回答下列问题:
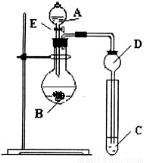
(1)图中E装置名称是_____________。
(2) N、C、Si的非金属性由强到弱的顺序是:_____________;从以下所给物质中选出甲同学设计的实验所用到物质:试剂A为_______;试剂C为_________(填序号)。
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
(3) 乙同学设计的实验中(酒精灯加热装置在图中未画出),若试剂C为溴化钾溶液溶液外,还需要用到的试剂有:试剂A为________;试剂B为 ________。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高二化学试卷(解析版) 题型:选择题
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都属于离子型碳化物。请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是
A.ZnC2水解生成乙烷B.Al4C3水解生成丙炔
C.Mg2C3水解生成丙炔 D.Li2C2水解生成乙烯
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高一化学试卷(解析版) 题型:选择题
下列物质中,不能和氯气发生取代反应的是
A.CH3Cl B.CCl4 C.CH2Cl2 D.CH4
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高一化学试卷(解析版) 题型:选择题
元素Y的原子获得3个电子或元素X的原子失去2个电子后,它们的电子层结构与氖原子的电子层结构相同,X、Y两种元素的单质在高温下得到的化合物的正确化学式是
A.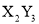 B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省黄石市秋季高二化学期中统考试卷(解析版) 题型:填空题
(10分)已知:用惰性电极电解某盐X的溶液,发生的反应为:
X+H2O  A(单质)+B(单质)+Y(化合物)
A(单质)+B(单质)+Y(化合物)
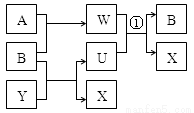
(1)若组成X的元素均为短周期元素,且A、B均为气体,其在相同条件下体积 比为1:1,产物之间可以发生如图的反应(变化中的水略去)。写出有关反应的离子反应方程式:①_______________________________。
(2)若A为红色固体,A可以与Y的浓溶液反应生成一种与A的摩尔质量相同的气体。
①写出该电解过程中阳极的电极反应式:___________________;
②某学生电解一定浓度的X溶液一段时间后,向所得溶液中加入0.1molACO3后,恢复到电解前的浓度和pH(不考虑CO2溶解),则电解过程中转移的电子数为_______。
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,且存在如下的转化关系:
Ⅰ. A+Y(浓)→X+C(气体)+H2O;Ⅱ. A+Y(稀)→X+D(气体)+H2O;Ⅲ. M+O2→D(气体)+H2O。
①已知:组成M气体的两种元素质量比为14:3,则检验M的方法是___________________;
②在标准状况下,27gA溶于一定浓度的Y溶液时,产生2.8L气体,将装有该气体的量筒倒立于有水的水槽中,再通入_______L气体B,水才能恰好充满量筒。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省黄石市秋季高二化学期中统考试卷(解析版) 题型:选择题
一定温度下,某密闭容器里发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g) (正反应为放热反应),当反应达到平衡时,测得容器中各物质的物质的量均为 n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施可采用的是( )
CO2(g)+H2(g) (正反应为放热反应),当反应达到平衡时,测得容器中各物质的物质的量均为 n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施可采用的是( )
①升高温度 ②增大压强
③再通入n mol CO2和n mol H2 ④再加入2n mol CO和2n mol H2O(g)
A.①② B.②④ C.③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省高三5月模拟考试理综化学试卷(解析版) 题型:选择题
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是:

A.该电池为可充电池
B.每有0.1molO2反应,则迁移0.4mol
C.正极反应式为:CH2=CH2-2e-+2OH-=CH3CHO+H2O
D.电子移动方向:电极a→磷酸溶液 →电极b
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:实验题
(14分)
某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:
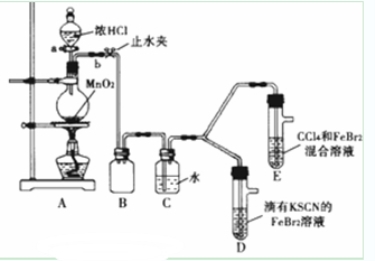
(1)①检查气体发生装置A的气密性的操作是:____________
②整套实验装置存在一处明显不足,请指出_____________.
(2)用改正后的装置进行实验.实验过程如下:
实验操作 | 实验现象 | 结论 |
打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯 | D装置中:溶液变红 E装置中:水层溶液变黄振荡后CCl4层无明显变化 | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: ______________________ |
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化:
D装置中:红色慢慢褪去。E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深最后变成红色。为探究上述实验现象的本质,小组同学查得资料如下:
Ⅰ.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2. Ⅱ.Cl2和Br2反应生成BrCl,它呈红色(略带黄色),沸点为5℃,与水发生水解反应. Ⅲ.AgClO、AgBrO均可溶于水. |
①请用平衡移动原理(结合化学用语)解释Cl2过量时D中溶液红色褪去的原因___________________,请设计简单实验证明上述解释:______________________
②欲探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生.请结合化学用语解释仅产生白色沉淀的原因_______________________________________________
③将少量BrCl通入到碘化钾溶液中,该反应的化学方程式为:___________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com