
| A、c(Cl-)>c(H-)>c(NH4+)>c(OH-) |
| B、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、c(Cl-)>c(OH-)>c(NH4+)>c(H+) |
| D、c(Cl-)>c(NH4+)>c(OH-)>c(H+) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸式滴定管滴至终点,俯视读数 |
| B、碱液移入锥形瓶后,加入10mL蒸馏水 |
| C、酸式滴定管注入酸溶液后,尖嘴无气泡时开始滴定,滴定后有气泡 |
| D、酸式滴定管用蒸馏水洗涤后,未用标准液润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4+2O2=CO2+2H2O△H═-889.6kJ/mol |
| B、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+889.6kJ/mol |
| C、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-55.6kJ/mol |
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸中滴加氨水至中性,溶质为氯化铵 |
| B、稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 |
| C、饱和石灰水中加入少量CaO,恢复至原温后溶液的pH值不变 |
| D、向沸水中滴加适量饱和FeCl3溶液,可制得红褐色带电的胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl BaSO4 |
| B、KNO3 CH3COOH |
| C、HCl NaHSO4 |
| D、NH3?H2O H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
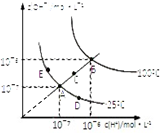
| A、图中五点KW间的关系:B>C>A=D=E |
| B、若从A点到D点,可采用:温度不变时在水中加入少量酸 |
| C、在B点对应的温度下,将pH=2的硝酸与pH=10的Ba(OH)2(aq)等体积混合后,溶液显中性 |
| D、若从A点到C点,可采用:温度不变时在水中加入适量的NH4Cl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两溶液溶质物质的量浓度相同 |
| B、用同浓度的盐酸中和时,消耗盐酸的体积相同 |
| C、两溶液中OH-离子浓度相同 |
| D、加入等体积的水稀释后,它们的pH仍相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com