
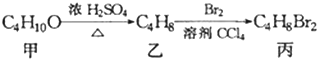 ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )| A. | CH3CH(CH2Br)2 | B. | (CH3)2CBrCH2Br | C. | C2H5CHBrCH2Br | D. | CH3(CHBr)2CH3 |
分析 由甲与乙的分子式可知,丁醇发生消去反应生成丁烯,丁烯与溴发生加成反应,两个溴原子应分别连接在相邻的碳原子上,得到二溴丁烷,判断出C4H8的烯烃的同分异构体进行解答.
解答 解:C4H8属于烯烃的可能的同分异构体,有CH2═CH2CH2CH3、CH3CH═CHCH3、CH2═C(CH3)2.
A.C4H8为烯烃,与溴发生加成反应后溴原子处于相邻的2个碳原子上,故A错误;
B.若乙为CH2═C(CH3)2,与溴发生加成反应生成(CH3)2CBrCH2Br,故B正确;
C.若乙为CH2═CH2CH2CH3,与溴发生加成反应生成CH3CH2CHBrCH2Br,故C正确;
D.若乙为CH3CH═CHCH3,与溴发生加成反应生成CH3CHBrCHBrCH3,故D正确;
故选A.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断及发散思维能力,关键判断C4H8属于烯烃的可能的同分异构体及理解加成反应机理,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有8个中子的氧原子:18O | B. | Na2O的电子式: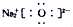 | ||
| C. | HClO 的结构式:H一CI一O | D. | F一的结构示意图: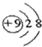 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X和Y形成化合物时,X显负价,Y显正价 | |
| B. | 第一电离能Y可能小于X | |
| C. | 最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性 | |
| D. | 气态氢化物的稳定性:HmY大于HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氯化铁溶液鉴别苯酚溶液、辛烯、溴苯和乙醇四种有机物 | |
| B. | 用溴水鉴别苯、辛烯、甲苯和乙醇四种有机物 | |
| C. | 用酸性高锰酸钾溶液鉴别苯、甲苯、硝基苯四种液态有机物 | |
| D. | 用硫酸铜溶液除去乙炔中的杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤、预期现象 | 结论 |
| ①向溶液中加入适量苯,振荡、静置后 现象:CCl4层呈橙红色. | 假设1正确 |
| ②向溶液中加入KSCN溶液溶液 现象:溶液变为红色. | 假设2正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
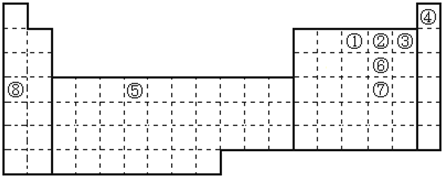
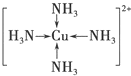 .
.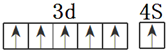 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com