
 (Ⅰ)开发新型替代燃料成为各国关注的重要科研项目,中国现已成为世界第三大利用植物秸秆(主要成分纤维素)生产燃料乙醇的国家.写出乙醇燃烧的化学方程式:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(Ⅰ)开发新型替代燃料成为各国关注的重要科研项目,中国现已成为世界第三大利用植物秸秆(主要成分纤维素)生产燃料乙醇的国家.写出乙醇燃烧的化学方程式:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.分析 (Ⅰ)乙醇为清洁能源,可燃烧生成二氧化碳和水;
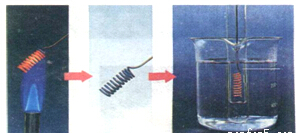
(Ⅱ)(1)增大了铜丝的接触面积,加快反应速率;
(2)铜在空气中燃烧,由红色变为黑色,插入乙醇中时由黑色变为红色.
解答 解:(Ⅰ)乙醇燃烧生成二氧化碳和水,燃烧的化学方程式是C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,
故答案为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
(Ⅱ)(1)铜丝绕成螺旋状的作用是:增大了铜丝的接触面积,加快反应速率
故答案为:增大了铜丝的接触面积,加快反应速率;
(2)铜丝的颜色先后发生的变化是:铜丝在酒精灯上加热时由红色变为黑色,插入乙醇中时由黑色变为红色;反应方程式是:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O;
故答案为:铜丝在酒精灯上加热时由红色变为黑色,插入乙醇中时由黑色变为红色;2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的双基的考查,注意把握乙醇催化氧化的特点以及相关方程式的书写,难度不大.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:解答题
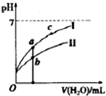 (1)25℃时,下列4种溶液.请回答下列问题.
(1)25℃时,下列4种溶液.请回答下列问题.| 物质 | H3PO2 | H2S | 一元酸HA |
| Kn | Kn=5.9×l0-2 | Kn1=9.1×l0-8 Kn2=l.l×l0-12 | Kn=l.1×1O-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
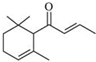 一种从植物中提取的天然化合物α-damascone可用于制作“香水”,其结构为:,有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物α-damascone可用于制作“香水”,其结构为:,有关该化合物的下列说法不正确的是( )| A. | 分子式为C13H20O | |
| B. | 该化合物可发生聚合反应 | |
| C. | 与溴的CCl4溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO3溶液检验 | |
| D. | 1 mol该化合物完全燃烧消耗19 molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
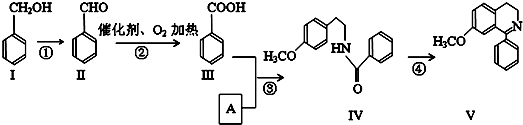
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2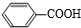 .
.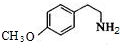 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S | B. | O2 | C. | SO2 | D. | SO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com