
| A. | 丁达尔现象可用来区别胶体与溶液 | |
| B. | 溶液、胶体、浊液的根本区别是分散质粒子直径的大小 | |
| C. | 胶体在一定条件下会发生聚沉 | |
| D. | 胶体粒子能通过半透膜,不能通过滤纸 |
分析 A.胶体具有丁达尔现象,溶液无此性质;
B.分散系本质区别是分散质微粒直径的不同;
C.胶体是介稳分散系,一定条件下发生聚沉;
D.胶体能通过滤纸,不能通过半透膜.
解答 解:A.胶体具有丁达尔现象,溶液无此性质,丁达尔现象可用来区别胶体与溶液,故A正确;
B.分散系本质区别是分散质微粒直径的不同,溶液中分散质直径小于1nm、胶体微粒直径1-100nm、浊液微粒直径大于100nm,所以根本区别是分散质粒子直径的大小,故B正确;
C.胶体是介稳分散系,一定条件下发生聚沉,如加入电解质溶液、加热、加入相反电荷的胶体等,故C正确;
D.胶体粒子是微粒集合体,能通过滤纸,不能通过半透膜,故D错误.
故选D.
点评 本题考查了胶体特征和性质的理解应用,掌握基础是关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,B:
,B: ,C:
,C: .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
 A结构式CH2=CH2
A结构式CH2=CH2查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:请回答:
原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:请回答: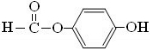 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com