
���ݻ�������ܱ������д������·�Ӧ��2SO2��g��+O2��g��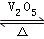 2SO3��g����H��0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ���ǣ� ��
2SO3��g����H��0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ���ǣ� ��
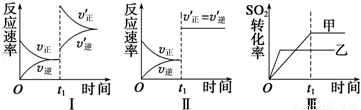
A��ͼ���ʾ����t1ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
B��ͼ���ʾ����t1ʱ�̼��������Է�Ӧ���ʵ�Ӱ��
C��ͼ���ʾ���Ǵ����Ի�ѧƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ�
D��ͼ���ʾ����ѹǿ�Ի�ѧƽ���Ӱ�죬���ҵ�ѹǿ�ϸ�
 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ��һ��ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڽ��������������ȷ����
A����ɫ�����ǹ��ܽ�
B�������ơ��̶������ܽ�
C������ֽ�ܰѽ����еķ�ɢ�����ɢ������
D��������С��1nm��100 nm֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶��϶ο��Ļ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Լ��У��ܺ��Ҵ�����������Ӧ����
A���� B��������� C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���ܱ�������A��B��Ӧ����C���䷴Ӧ���ʷֱ���v��A����v��B����v��C����ʾ����֪v��A����v��B����v��C��֮�������¹�ϵ2v��B��=3v��A����3v��C��=2v��B������˷�Ӧ�ɱ�ʾΪ�� ����
A��2A+3B=2C B��A+3B2=C C��3A+B=2C D��A+B=C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������ʡ�߶�����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��25��ʱ��AgCl�İ�ɫ����Һ�У����μ����Ũ�ȵ�KI��Һ��Na2S��Һ���۲쵽���������ȳ��ֻ�ɫ���������ճ��ֺ�ɫ��������֪�й����ʵ��ܶȻ�KSP��25�棩���£�
AgCl | Agl | Ag2S | |
KSP����λʡ�ԣ� | 1.8��10��10 | 1.5��10��16 | 1.8��10��50 |
��������������ǣ� ��
A������ת����ʵ�ʾ��dz����ܽ�ƽ����ƶ�
B���ܽ��С�ij�������ת��Ϊ�ܽ�ȸ�С�ij���
C��AgCl�����ڵ����ʵ���Ũ�ȵ�NaCl��CaCl2 ��Һ�е��ܽ����ͬ
D��25��ʱ���ڱ���AgCl��AgI��Ag2S��Һ�У�����Ag����Ũ�Ȳ���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016��������������ѧԺ������ѧ�߶�����ĩ��ѧ���������棩 ���ͣ�ѡ����
����ˮ�������ϸ��¶ȣ�����������ȷ����
A��Kw���pH��С�������� B��Kw���pH���䡢������
C��Kw��С��pH��ʼ��� D��Kw���pH��С��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ�����ϵ����μ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ʵ�����ӷ���ʽ�����Ӧ��ϵ����ȷ����
A����Ag2S ��Һ�еμ�����ϡNaCl ��Һ����ɫ������ɰ�ɫ�� Ag2S +Cl�� AgCl +S2��
AgCl +S2��
B����K2Cr2O7 ��Һ�еμ�����ŨH2SO4����Һ��Ϊ��ɫ��
Cr2O72��(��ɫ) + H2O  2CrO42��(��ɫ) +2H+
2CrO42��(��ɫ) +2H+
C������۵⻯����Һ�еμ�ϡ���ᣬ�ڿ����з���һ��ʱ�����Һ������
4H+ + 4I- + O2 �� 2I2 + 2H2O
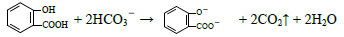
D����ˮ����(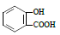 )�еμ�NaHCO3 ��Һ���ų���ɫ���壺
)�еμ�NaHCO3 ��Һ���ų���ɫ���壺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶�����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
�������˻ᡰ���ơ����ȼ���DZ���(C3H8)������������˻���ȼ���DZ�ϩ(C3H6)��
��1����������ɵñ�ϩ��
��֪��C3H8(g)�TCH4(g)+HC��CH(g)+H2(g)��H1=+156.6kJ/mol
CH3CH=CH2(g)�TCH4(g)+HC��CH(g)��H2=+32.4kJ/mol
����ͬ�����£���ӦC3H8(g)�TCH3CH=CH2(g)+H2(g)�ġ�H= kJ��mol��1��
��2���Ա���Ϊȼ����������ȼ�ϵ�أ���ص�����ͨ��O2��CO2������ͨ����飬�����������̼���Ρ���ط�Ӧ����ʽΪ ���ŵ�ʱCO32�������ص� (���������)����
��3��̼�⻯������ȫȼ������CO2��H2O�����³�ѹ�£������е�CO2����ˮ���ﵽƽ��ʱ����Һ��pH =5.60��c(H2CO3)=1.5��10-5 mol��L-1��������ˮ�ĵ��뼰H2CO3�ĵڶ������룬��H2CO3 HCO3����H����ƽ�ⳣ��K1= mo1/L��(��֪10-5.60=2.5��10-6)
HCO3����H����ƽ�ⳣ��K1= mo1/L��(��֪10-5.60=2.5��10-6)
��4�������£�0.1 mo1/L NaHCO3��Һ��pH����8������Һ��c(H2CO3) c(CO32��)(�����������������)��ԭ���� (�ü�Ҫ��������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ��������ĩ��ѧ�Ծ��������棩 ���ͣ�ʵ����
��ͼ1��ʢ������Լ�ƿ�ϵı�ǩ�IJ������ݣ���ʵ����Ҫ0.5 mol•L-1H2SO4��Һ480mL��������������������Һ�������ʵ�������е�������ҩƷ����ش��������⣺
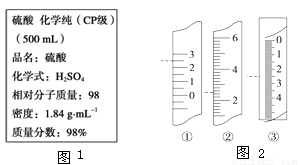
��1������ƿӦ��μ�©____________________________________��
��2��ʵ���г���Ͳ���ձ����Ҫ����������________________��
��3����������Ũ��������ԼΪ______mL��������������������ˮ��ϣ�������Һ�����ʵ���������__________49%�����������=����������
��4�����в���������������ҺŨ��ƫ�����_______������ĸ����
A������Ͳ��ȡŨ����ʱ��������Ͳ�Ŀ̶�
B��������ƿ��ת��ʱ����Һδ��ȴ
C������ʱ���ӿ̶���
D�����ݺ���ҡ�Ⱥ�������ʱ������Һ����ڿ̶���
��5���¶ȼơ���Ͳ���ζ��ܵ�һ������ͼ2��ʾ������������������ָ�̶ȣ���˵����ȷ����_____ ������ĸ����A��������Ͳ������Ϊ2.5mLB��������Ͳ������Ϊ2.5mLC�����ǵζ��ܣ�����Ϊ2.5mLD�������¶ȼƣ�����Ϊ2.5��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com