
【题目】某合金只含铝、铁、铜三种元素,取合金![]() ,加入到含
,加入到含![]() 稀硝酸的溶液中,恰好完全反应,放出无色气体
稀硝酸的溶液中,恰好完全反应,放出无色气体![]() 标准状况下
标准状况下![]() 。将反应后的溶液分成2等份,向一份溶液中滴加
。将反应后的溶液分成2等份,向一份溶液中滴加![]() ,无明显现象。向另一份溶液中滴加氨水至过量,过滤得沉淀bg,充分灼烧得固体
,无明显现象。向另一份溶液中滴加氨水至过量,过滤得沉淀bg,充分灼烧得固体![]() ,减轻了
,减轻了![]() ,再加入到过量的
,再加入到过量的![]() 溶液中,剩余不溶物
溶液中,剩余不溶物![]() 。下列说法不正确的是
。下列说法不正确的是![]()
![]()
已知:![]() 遇到
遇到![]() 会出现蓝色沉淀;
会出现蓝色沉淀; ![]()
A.![]()
B.原合金中铜的质量为![]()
C.若将上述![]() 稀硝酸逐滴加入到合金中,放出气体仍为
稀硝酸逐滴加入到合金中,放出气体仍为![]() 标准状况下
标准状况下![]()
D.d不是一确定值,可能为8
【答案】D
【解析】
A.将反应后的溶液分成2等份,一份溶液中滴加![]() 溶液,无明显现象,则不含
溶液,无明显现象,则不含![]() ,所以溶液为
,所以溶液为![]() 、
、![]() 、
、![]() 的混合液。在另一份溶液中滴加氨水至过量,得到沉淀
的混合液。在另一份溶液中滴加氨水至过量,得到沉淀![]() 为
为![]() 和
和![]() ,
,![]() 则转变为
则转变为![]() ,过滤后进入滤液。固体
,过滤后进入滤液。固体![]() 为
为![]() 和
和![]() ,不溶物
,不溶物![]() 为
为![]() ,合金加入到硝酸溶液后,放出无色气体
,合金加入到硝酸溶液后,放出无色气体![]() 标准状况下
标准状况下![]() 即
即![]() ,根据得失电子守恒,合金总共失去电子
,根据得失电子守恒,合金总共失去电子![]() ,反应后溶液中阳离子带正电荷
,反应后溶液中阳离子带正电荷![]() ,所以溶液中硝酸根
,所以溶液中硝酸根![]() ,所以
,所以![]() ,A正确;
,A正确;
B.根据电子守恒可知:![]() ,合金总质量为:
,合金总质量为:![]() ,固体减少的
,固体减少的![]() 为氢氧化铝、氢氧化铁分解生成的水,则
为氢氧化铝、氢氧化铁分解生成的水,则![]() ,固体
,固体![]() 和
和![]() 中H元素的物质的量之和等于:
中H元素的物质的量之和等于:![]() ,可得
,可得![]() ,原固体中
,原固体中![]() ,
,![]() ,则
,则![]() ,所以
,所以![]() ,B正确;
,B正确;
C.由于溶液中不含![]() ,为
,为![]() 、
、![]() 、
、![]() 的混合液,所以硝酸足量,若将上述nmol稀硝酸逐滴加入到合金中,先生成
的混合液,所以硝酸足量,若将上述nmol稀硝酸逐滴加入到合金中,先生成![]() ,后
,后![]() 继续被硝酸氧化,由于硝酸足量,最终生成
继续被硝酸氧化,由于硝酸足量,最终生成![]() 、
、![]() 、
、![]() ,根据得失电子守恒生成的NO气体仍为
,根据得失电子守恒生成的NO气体仍为![]() ,C正确;
,C正确;
D.最后剩余不溶物dg,为![]() ,是一确定值,D错误。
,是一确定值,D错误。
故选D。


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】有Ⅰ~Ⅳ四个体积均为 0.5 L 的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入 HCl 和 O2(如下表),加入催化剂发生反应 4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
容器 | 起始时 | ||
t/℃ | n(HCl)·mol-1 | Z | |
I | 300 | 0.25 | a |
II | 300 | 0.25 | b |
III | 300 | 0.25 | 4 |
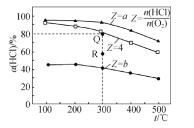
A.ΔH<0,b<4<a
B.300 ℃该反应的平衡常数的值为 64
C.容器Ⅲ某时刻处在 R 点,则 R 点的 v 正>v 逆,压强:p(R)>p(Q)
D.若起始时,在容器Ⅳ中充入 0.25 mol Cl2 和 0.25 mol H2O(g),300 ℃达平衡时容器中 c(HCl)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是形成酸雨的罪魁祸首之一,含硫煤燃烧的尾气处理一直是化学研究的重要课题。某工厂设计了新的治污方法,该工艺流程如图所示,下列叙述不正确的是( )
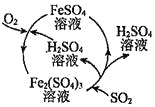
A.该过程中可得到化工产品![]()
B.该工艺流程中![]() 可以循环利用
可以循环利用
C.若处理含![]() 的尾气,理论上需要通入相同条件下的空气约
的尾气,理论上需要通入相同条件下的空气约![]()
D.可用澄清石灰水检验最终排出的气体是否含有二氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟及其化合物用途非常广泛。回答下列问题:
(1)基态锑(Sb)原子价电子排布的轨道式为____。[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,该离子的空间构型为______,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_______、_________。
(2)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____(填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_____。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______(填序号):
A 离子键 B σ键 C π键 D 配位键 E 范德华力
(3)某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为![]() ,该晶体的密度ρ_________g·cm-3。
,该晶体的密度ρ_________g·cm-3。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脱硫技术能有效控制SO2对空气的污染。
(1)向煤中加入石灰石可减少燃烧产物中SO2的含量,该反应的化学方程式是
_______________________________。
(2)海水呈弱碱性,主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42—、Br-、HCO3—等。含SO2的烟气可利用海水脱硫,其工艺流程如图所示:

①向曝气池中通入空气的目的是_____________________________________。
②通入空气后曝气池中海水与天然海水相比,浓度有明显不同的离子是________。
a.Cl- b.SO42— c.Br- d.HCO3—
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可得到NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。

①图中a极要连接电源的________(填“正”或“负”)极,C口流出的物质是________。
②SO32—放电的电极反应式为____________________________。
③电解过程中阴极区碱性明显增强,用平衡移动的原理解释原因:
__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A2 + 3B2(?)![]() 2AB3(g)中,AB3的百分含量(w)与温度和压强的关系如图所示。下列说法正确的是( )
2AB3(g)中,AB3的百分含量(w)与温度和压强的关系如图所示。下列说法正确的是( )
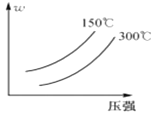
A.该反应为吸热反应
B.反应物B2为气体
C.升高温度,逆反应速率减慢
D.增大压强,A2转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种粒子中,半径按由大到小排列顺序正确的是
①基态X的原子结构示意图
②基态Y的价电子排布式:3s23p5
③基态Z2-的电子排布图![]()
④W基态原子有2个能层,电子式为![]()
A. ①>②>③>④ B. ③>④>①>②
C. ③>①>②>④ D. ①>②>④>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铁矿石、焦炭、空气、石灰石为原料来冶炼铁。
(1)请写出用磁铁矿在高温下冶炼铁的化学方程式___________。请你用化学方法设计实验方案检验上述反应得到的固体产物中含有铁粉___________。
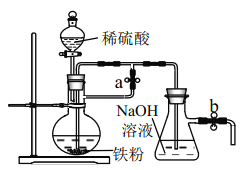
(2)小明同学将用冶炼所得的铁粉按下图装置来制备 Fe(OH)2,实验开始时应先_______活塞a,___________活塞 b(填“打开”或“关闭”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室进行铁盐与亚铁盐相互转化的实验:
实验Ⅰ:将![]() 转化为
转化为![]() 如图
如图![]()
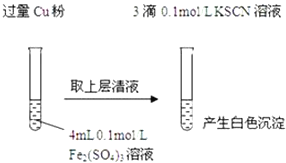
(1)Fe3+与Cu粉发生反应的离子方程式为______.
(2)探究白色沉淀产生的原因,请填写实验方案:查阅资料:
![]() 的化学性质与
的化学性质与![]() 相似,
相似,![]() 白色
白色![]()
实验方案 | 现象 | 结论 |
步骤1:取4mL ______ | 产生白色沉淀 |
|
步骤2:取 ______ | 无明显现象 |
![]() 与
与![]() 反应的离子方程式为______.
反应的离子方程式为______.
实验Ⅱ:将![]() 转化为
转化为![]()
实验方案 | 现象 |
向3mL | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
探究上述现象出现的原因:查阅资料:![]() 棕色
棕色![]()
(3)用离子方程式解释NO产生的原因______.
(4)从化学反应速率与限度的角度对体系中存在的反应进行
反应Ⅰ:![]() 与
与![]() 反应;反应Ⅱ:
反应;反应Ⅱ:![]() 与NO反应
与NO反应
①依据实验现象,甲认为反应Ⅰ的速率比反应Ⅱ______![]() 填“快”或“慢”
填“快”或“慢”![]() .
.
②乙认为反应Ⅰ是一个不可逆反应,并通过实验证明其猜测正确,乙设计的实验方案是______.
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com