
 �״�ȼ�ϵ�ر���Ϊ��21���͵綯������Ѻ�ѡ����Դ��
�״�ȼ�ϵ�ر���Ϊ��21���͵綯������Ѻ�ѡ����Դ������ ��1������ȼ���ȸ�����1mol��ȼ����ȫȼ�������ȶ�������ų����������������������Ȼ�ѧ����ʽ��д��������ע���ʾۼ�״̬�Ͷ�Ӧ�ʱ䣻
��2���ɸ�˹���ɿ�֪����CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H1=+49.0kJ•mol-1����H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-241.8kJ•mol-1����+�۵õ���Ӧ�ڣ�
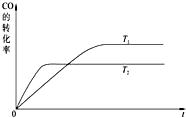
��3�������ȹ���ƽԭ����ͼ1��֪���¶�T1��T2��ƽ��ʱ���¶�Խ��CO��ת����ԽС��˵�������¶ȣ�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ����ݴ��жϷ�Ӧ�ȣ�K1��K2��ϵ��
��� �⣺��1����25�桢101kPa�£�1mol CH3OHҺ����ȫȼ������CO2��Һ̬ˮʱ�ų�����726.51kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-725.76kJ•mol-1��
�ʴ�Ϊ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-725.76kJ•mol-1��
��2���ɸ�˹���ɿ�֪����CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H1=+49.0kJ•mol-1����H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-241.8kJ•mol-1����+�۵õ���Ӧ�ڣ����H2=+49.0kJ•mol-1+��-241.8kJ•mol-1��=-192.8kJ•mol-1���ʴ�Ϊ��-192.8kJ•mol-1��
��3���ٸ����ȹ���ƽԭ����ͼ1��֪���¶�T1��T2��ƽ��ʱ���¶�Խ��CO��ת����ԽС��˵�������¶ȣ�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ����ʸ÷�Ӧ����ӦΪ���ȷ�Ӧ���ʴ�Ϊ������
��ƽ��ʱ���¶�Խ��CO��ת����ԽС��˵�������¶ȣ�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ�ƶ����ʸ÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�ƶ�������K1��K2��
�ʴ�Ϊ������
���� ����Ϊ�ۺ��⣬�漰�Ȼ�ѧ��Ӧ����ʽ����д����ѧ��Ӧ���ʺ�ƽ���ƶ���Ӱ�����ص�֪ʶ�㣬ע�ظ߿���������Ŀ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
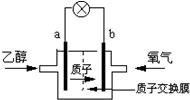
| A�� | a��Ϊ��صĸ������Ҵ�����ԭ | |
| B�� | ��ع���ʱ������b���ص��߾������ٵ�a�� | |
| C�� | ��������ĵ缫��ӦΪ��2H++O2+4e-=H2O | |
| D�� | ��ع���ʱ1mol�Ҵ�������ʱ������12mol����ͨ�����ӽ���Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������һ�����ڷ�Ӧ�������� | |
| B�� | ���ȷ�Ӧ���ؼ��Ⱦ�һ���ܷ��� | |
| C�� | Ӧ�ø�˹���ɣ��ɼ���ijЩ����ֱ�Ӳ����ķ�Ӧ���ʱ� | |
| D�� | ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����ġ�H��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��λʱ��������n mo1 O2��ͬʱ����2n mol NO2 | |
| B�� | ����������ɫ���ٸı� | |
| C�� | ��������ѹǿ���ٸı��״̬ | |
| D�� | ���������ܶȲ��ٸı��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Тٻ�� | B�� | ֻ�Тڻ�� | C�� | ֻ�Тٻ�ڻ�� | D�� | �٢ڢۢ�������һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �պ��ľ̿���ȵ�Ũ���� | B�� | ͭ��Ũ���Ṳ�� | ||
| C�� | ʳ�κ�Ũ���Ṳ�� | D�� | �����е���Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com