
��ѧ�������ǽ��������ģ�����˵����ȷ����(����)
A��Ϊ��ֹ�����±��ȸ�֬ʳƷ�������ʣ����ڰ�װ���з�����ʯ��
B����ˮ�����ܽ����ˮ��ӦΣ������ˮ�мӾ�ˮ����������ʹ��ˮ����
C�������ڳ�ʪ�Ŀ����������⣬�为����ӦʽΪ2H2O��O2��4e��===4OH��
D���������ȼ����Ҫ��ѹ����Ȼ����Һ��ʯ�������࣬���Ǿ�����̼�⻯����
 ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д� ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ijʵ��С���H2O2�ķֽ���������̽�����±��Ǹ�ʵ��С���о�Ӱ��H2O2�ֽ����ʵ�����ʱ��¼��һ�����ݣ���������ͬ��״̬��ͬ��MnO2�ֱ����ʢ��15 ml 5%��H2O2��Һ�Ĵ��Թ��У����ô����ǵ�ľ�����ԣ�������£�
| MnO2 | �����Թ���� | �۲��� | ��Ӧ��������ʱ�� |
| ��ĩ״ | ���� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5 |
| ��״ | �� | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30min |
��1��
д�����Թ��з�����Ӧ�Ļ�ѧ����ʽ�� ��
�÷�Ӧ�� ��Ӧ������Ȼ����ȣ���
��2��ʵ���������������Ĵ�Ч���� �йء�
��ij���淴Ӧ��ij���Ϊ5L���ܱ������н��У� �ڴ�0��3���Ӹ����ʵ����ı仯�����ͼ��ʾ��A,B,C��Ϊ���壩��
 ��3���÷�Ӧ�ĵĻ�ѧ����ʽΪ ��
��3���÷�Ӧ�ĵĻ�ѧ����ʽΪ ��
��4����Ӧ��ʼ��2����ʱ��B��ƽ����Ӧ����Ϊ ��
��5����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ��
a��v(A)= 2v(B) b��������ѹǿ���ֲ���
c��v��(A)= v��(C) d�������ڻ��������ܶȱ��ֲ���
��6������ͼ���A��ƽ��ʱ��ת����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ⱦ�뻷�������Ѿ���Ϊ�����ҹ������ŵ�һ�����⣬��Ⱦ��Ϊ������Ⱦ��ˮ��Ⱦ��������Ⱦ�ȡ�
��1��Ϊ�˼��ٿ�����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
�ٽ�úת��Ϊ�������ȼ�ϡ�
��֪��H2(g)��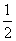 O2(g)===H2O(g) ��H1����241.8 kJ��mol��1
O2(g)===H2O(g) ��H1����241.8 kJ��mol��1
C(s)��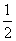 O2(g)===CO(g) ��H2����110.5 kJ��mol��1
O2(g)===CO(g) ��H2����110.5 kJ��mol��1
д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ�� �� ��
�÷�Ӧ��ƽ�ⳣ������ʽΪK�� �� ��
��ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ����� �� ��ѡ����ţ���
a��Ca(OH)2 b��CaCl2 c��Na2CO3 d��NaHSO3
��2��Ϊ�˼��ٿ����е�CO2��Ŀǰ��̼�����ڽ������������ŷ��о�����Ҫ�����ã���̼������(NH4)2CO3����ӦΪ��(NH4)2CO3(aq)��H2O(l)��CO2(g)��2NH4HCO3(aq) ��H3
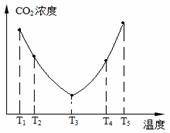 Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�
Ϊ�о��¶ȶ�(NH4)2CO3����CO2Ч�ʵ�Ӱ�죬��ij�¶�
T1�£���һ������(NH4)2CO3��Һ�����ܱ������У�����
��һ������CO2���壨�õ�����Ϊϡ�ͼ�������tʱ�̣�
���������CO2�����Ũ�ȡ�Ȼ��ֱ����¶�ΪT2��T3��
|
������ͬʱ����CO2����Ũ�ȣ����ϵ��ͼ7����
�٦�H3 �� 0(�����������������)��
����T4��T5����¶����䣬������CO2����Ũ�ȱ仯���Ƶ�ԭ���ǣ� �� ��



 ��3�������������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
��3�������������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
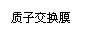 �ٴ����������У���H2��NO
�ٴ����������У���H2��NO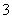 ��ԭΪN2��һ��ʱ���
��ԭΪN2��һ��ʱ���
��Һ�ļ���������ǿ����Ӧ���ӷ���ʽΪ�� �� ��
|
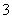 ��ԭ����ͼ8����Դ����Ϊ�� ��
��ԭ����ͼ8����Դ����Ϊ�� �� ��ѡ���A����B������������ӦʽΪ�� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݱ����ṩ�IJ��ֶ�����Ԫ��ԭ�Ӱ뾶����Ҫ���ϼ۵���Ϣ���ж�������������ȷ���ǣ�
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| ��Ҫ���ϼ� | ��2 | ��3 | ��2 | ��6����2 | ��2 |
A. �⻯��ķе�ΪH2T<H2R B��������ϡ���ᷴӦ������ΪL��Q
C��M��T�γɵĻ������������ D��L2����R2���ĺ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͪ�������ƹ��IJ���ҩ����������½ṹ��ʽ��

���й�����ͪ�����������������(����)
A�������ڴ��������º��巴Ӧ
B�����Ժ�������Һ����������Ӧ
C����һ�������¿��Է�����ȥ��Ӧ
D�����Ժ�Ũ������Ũ����Ļ��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ѧ��ѡ��5�л���ѧ������(15��)
�л���H��һ�ֺϳ�ҩ����м��壬H�ĺϳɷ������£�

��ش��������⣺
��1��A����Է�������Ϊ104�ķ�������A�ķ���ʽΪ ��
��2������A��C�����л����Լ�Ϊ ��
��3��FΪһ�ȴ����˴Ź����������������շ壬��E�Ľṹ��ʽΪ ��
��4��д��B��C�Ļ�ѧ����ʽ�� ��
��5��д��D��G����H�Ļ�ѧ����ʽ�� ��
��6��D��ͬ���칹��������FeCl3��Һ������ɫ��Ӧ���ܷ���������Ӧ���� �֣�д�����к����������������շ���Ŀ���ٵĽṹ��ʽ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���³�ѹ�£���x mol CO2����ͨ��1 L y mol/L��NaOH��Һ�У����ж�������Һ ����������ȷ��
A����x��2yʱ������CO2�����ͨ�룬��Һ��
��ˮ�������c(H��)������ͼ�仯��ϵ
B����x��yʱ��������Һ�д��ڣ�
c(OH��)+c(CO32��)��c(H��)+c(H2CO3)
C����2x��yʱ��������Һ�д��ڣ�
c(Na��)��c(CO32��)��c(OH��)��c(HCO3��)��c(H��)
D����1/2��x/y��1ʱ��������Һ��һ�����ڣ�
c(Na��)��c(CO32��)+c(HCO3��)+c(H2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ƭ��ϡ���ᷴӦʱ�����д�ʩ����ʹ��Ӧ���ʼӿ����
A������ B���μ�������CuSO4��Һ
C������ϡ���ᣬ����98%Ũ���� D��������Ƭ����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com