
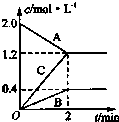
 如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:
如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:分析 (1)根据图知,随着反应的进行,物质的量浓度减小的物质是反应物、物质的量浓度增大的物质是生成物;
(2)该反应中△c(A)=(2.0-1.2)mol/L=0.8mol/L、△c(B)=(0.4-0)mol/L=0.4mol/L、△c(C)=(1.2-0)mol/L=1.2mol/L,同一反应中同一时间内,各物质物质的量浓度变化量之比等于其计量数之比,所以A、B、C的计量数之比=0.8mol/L:0.4mol/L:1.2mol/L=2:1:3,据此书写方程式;
(3)可逆反应达到平衡状态时各物质的物质的量浓度不变;B的平均反应速率=$\frac{△c}{△t}$;A的转化率=$\frac{△c(A)}{c(A)}$×100%.
解答 解:(1)根据图知,随着反应的进行,物质的量浓度减小的物质是反应物、物质的量浓度增大的物质是生成物,所以A是反应物、B和C是生成物,故答案为:A;
(2)该反应中△c(A)=(2.0-1.2)mol/L=0.8mol/L、△c(B)=(0.4-0)mol/L=0.4mol/L、△c(C)=(1.2-0)mol/L=1.2mol/L,同一反应中同一时间内,各物质物质的量浓度变化量之比等于其计量数之比,所以A、B、C的计量数之比=0.8mol/L:0.4mol/L:1.2mol/L=2:1:3,则该反应方程式为2A?B+3C,
故答案为:2A?B+3C;
(3)可逆反应达到平衡状态时各物质的物质的量浓度不变,根据图知,2min时该反应达到平衡状态;B的平均反应速率=$\frac{△c}{△t}$=$\frac{0.4mol/L}{2min}$=0.2mol/(L.min);A的转化率=$\frac{△c(A)}{c(A)}$×100%=$\frac{0.8mol/L}{2.0mol/L}×100%$=40%,
故答案为:2min;0.2mol/(L.min);40%.
点评 本题考查图象分析,侧重考查学生分析计算能力,明确浓度变化量与计量数关系是解本题关键,知道反应速率、转化率基本公式,题目难度不大.


科目:高中化学 来源: 题型:解答题
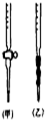 阅读下列实验内容,根据题目要求回答问题:
阅读下列实验内容,根据题目要求回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶内壁沾有水滴没有烘干就进行配制 | |
| B. | 转移液体时有少量洒落 | |
| C. | 量取浓硫酸时仰视刻度线 | |
| D. | 定容摇匀后液面下降再加水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有③④ | C. | 只有①③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| B. | 甲烷、乙烯和苯都能与酸性高锰酸钾溶液反应 | |
| C. | 乙酸乙酯和油脂在一定条件下都能水解 | |
| D. | 所有烷烃中都存在碳碳单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
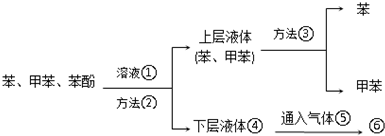
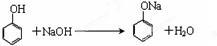 .
.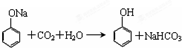 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图装置是实验室里常见的气体发生装置,用该装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
如图装置是实验室里常见的气体发生装置,用该装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )| 气体 | a | b | c | |
| A | NO2 | 浓硝酸 | 铜片 | NaOH溶液 |
| B | SO2 | 浓硫酸 | K2SO3粉末 | 浓硫酸 |
| C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| D | CO2 | 稀硫酸 | CaCO3粉末 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.00 | 20.01 |
| 2 | 1.00 | 20.99 |
| 3 | 0.00 | 21.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com