
在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+ 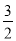 O2(g) = SO2(g)+H2O(g) △H 1
O2(g) = SO2(g)+H2O(g) △H 1
②2H2S(g)+SO2(g) =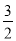 S2(g)+2H2O(g) △H 2
S2(g)+2H2O(g) △H 2
③H2S(g)+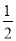 O2(g) = S(g)+H2O(g) △H 3
O2(g) = S(g)+H2O(g) △H 3
④S(g) = 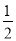 S2(g) △H4
S2(g) △H4
则△H 4的正确表达式为
A.△H 4 =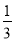 (3△H 3 - △H 1 - △H 2)
(3△H 3 - △H 1 - △H 2)
B. △H 4 =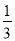 (△H 1 + △H 2 - 3△H 3)
(△H 1 + △H 2 - 3△H 3)
C.△H 4 =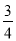 (△H 1 + △H 2 - 3△H 3)
(△H 1 + △H 2 - 3△H 3)
D.△H 4 =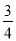 (△H 1 - △H 2 - 3△H 3)
(△H 1 - △H 2 - 3△H 3)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年湖北航天高中、安陆二中等五校高二上期中化学试卷(解析版) 题型:选择题
反应CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上学期期中测试化学试卷(解析版) 题型:选择题
只用一种试剂就可区别Na2SO4、AlCl3、FeCl3、MgSO4四种溶液。这种试剂是
A.HCl B.BaCl2 C.AgNO3 D.NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上学期10月月考化学试卷(解析版) 题型:选择题
下列溶液中Cl-浓度与50 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是
A.150 mL 1 mol·L-1的NaCl溶液
B.75 mL 2 mol·L-1 NH4Cl溶液
C.150 mL 2 mol·L-1的KCl溶液
D.75 mL 1 mol·L-1的FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A、取ag混合物充分加热,剩余bg固体
B、取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg
C、取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得bg固体
D、取ag混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得bg固体
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期期中测试化学试卷(解析版) 题型:选择题
在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g) 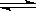 nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是
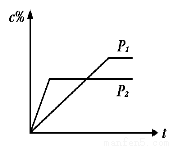
A.P1>P2,n<3 B.P1<P2,n>3
C.P1>P2,n>3 D.P1<P2,n<3
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江大庆实验中学高三上学期期中考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其它产物已略去).下列说法不正确的是( )

A.若甲是AlCl3溶液,则丁可能是NaOH溶液
B.若甲是Fe,则丁可能是Cl2
C.若丁是CO2,则甲可能为Mg
D.若丁是O2,则乙、丙的相对分子质量可能相差16
查看答案和解析>>
科目:高中化学 来源:2016届山西怀仁第一中学高三上学期期中考试化学试卷(解析版) 题型:推断题
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E同主族。某同学为探究甲的组成而进行如下实验:
①取mg甲的晶体溶于蒸馏水,配成500 mL溶液;
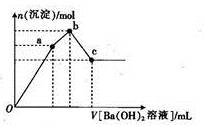
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20 mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224 mL。
回答下列问题:
(1)D在元素周期表中的位置为_ 。
(2)经测定晶体甲的摩尔质量为453 g·mol-1,其中阳离子和阴离子物质的量之比为1:1。 则晶体甲的化学式为_ _。
(3)图像中V(Oa):V(ab):V(bc)= _ 。
(4)写出ab段发生反应的离子方程式:_ 。
(5)配成的甲溶液物质的量浓度是_ 。
查看答案和解析>>
科目:高中化学 来源:2016届江苏常州一中、江阴南菁高中高三两校联考化学卷(解析版) 题型:填空题
NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得。工艺流程如下图:
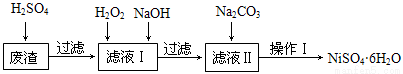
已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示。
Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
Ksp | 8.0×10—16 | 4.0×10—38 | 6.0×10—31 | 6.5×10—18 |
完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
注:NiCO3是一种不溶于水易溶于强酸的沉淀。
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有 。
A.升高反应温度 B.增大压强 C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是 (用离子方程式表示);
加入NaOH调节pH的范围是 ,为了除去溶液中的 离子。
(3)滤液Ⅱ的主要成分是 。
(4)检验Ni2+已完全沉淀的实验方法是 。
(5)操作Ⅰ的实验步骤依次为:
① ;
② ;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com