
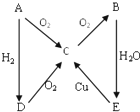
 如图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质.
如图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质.分析 (1)A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质,B为NO2,C被氧化生成B,则C是NO,A是气体单质,则A为N2,D为NH3,E为HNO3;
(2)氨气属于碱性气体,应该用碱性干燥剂干燥;
(3)B和水反应时生成硝酸和NO,B是氧化剂和还原剂,且氧化剂和还原剂的物质的量之比为1:2;
(4)氮气和氧气反应生成NO;氨气和氧气在催化剂加热条件下反应生成NO;氮气和氢气反应生成氨气.
解答 解:(1)A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质,B为NO2,C被氧化生成B,则C是NO,A是气体单质,则A为N2,D为NH3,E为HNO3;
通过以上分析知,B、C分别是NO2、NO,故答案为:NO2;NO;
(2)氨气属于碱性气体,应该用碱性干燥剂干燥,所以应该选取碱石灰作干燥剂,故答案为:碱石灰;
(3)B和水反应时生成硝酸和NO,B是氧化剂和还原剂,且氧化剂和还原剂的物质的量之比为1:2,故答案为:1:2;
(4)氮气和氧气反应生成NO,反应方程式为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;氨气和氧气在催化剂加热条件下反应生成NO,反应方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;氮气和氢气反应生成氨气,反应方程式为 N2+3H2$?_{高温高压}^{催化剂}$2NH3,故答案为:N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O; N2+3H2$?_{高温高压}^{催化剂}$2NH3.
点评 本题以N元素及其化合物之间的转化为载体考查无机物推断,以B的颜色及物质状态为突破口采用正逆结合的方法进行推断,熟练掌握常见物质颜色及其状态、物质之间的转化,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 硫氢化钠溶液中滴入硫酸铜溶液:S2-+Cu2+═CuS↓ | |
| B. | 稀硝酸中加入过量的铁粉:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O | |
| C. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 二氧化硫通入氯化铁溶液:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
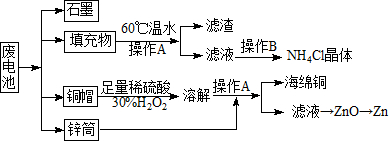 常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源
常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 剩余NO | B. | 剩余O2 | C. | 剩余NO2 | D. | 不剩余气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
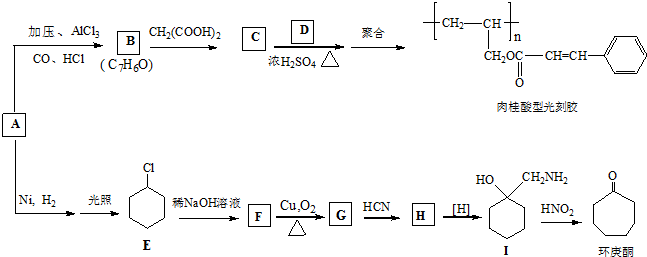
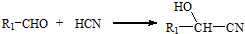
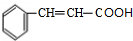 、CH2=CHCH2OH.
、CH2=CHCH2OH.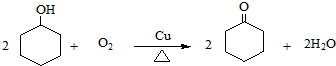 .
.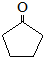 (环戊酮)为起始原料制备
(环戊酮)为起始原料制备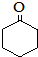 (环己酮)的合成路线.
(环己酮)的合成路线.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②③④ | C. | ②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
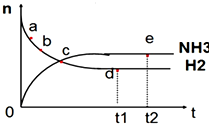 向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( )
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( )| A. | c点表示NH3生成速率与NH3分解速率相同 | |
| B. | c点和e点时反应的平衡常数相同 | |
| C. | N2的转化率:b>a | |
| D. | d点时,n(N2):n(H2):n(NH3)=1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油生产汽油的过程中没有发生化学变化 | |
| B. | 氮的固定过程中氮元素被氧化 | |
| C. | 葡糖糖转变成酒精的过程中产生的是水解反应 | |
| D. | 鸡蛋被煮熟的过程中发生的是蛋白质的变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com