
·ÖĪö æÉÓĆøßĆĢĖį¼ŲÓėÅØŃĪĖį·“Ó¦ÖʱøĀČĘų£¬Č»ŗóĘųĢåĶعż±„ŗĶŹ³ŃĪĖ®³żČ„ĀČ»ÆĒā£¬ÓĆĪŽĖ®ĀČ»ÆøĘøÉŌļ£¬ĶعżŹ¢ÓŠøÉŌļµÄÓŠÉ«²¼ĢõµÄ¼ÆĘųĘ棬æɹŪ²ģµ½ÓŠÉ«²¼Ģõ²»ĶŹÉ«£¬×īŗóÓĆÅű„ŗĶŹ³ŃĪĖ®µÄ·½·ØŹÕ¼ÆĀČĘų£¬ŅŌ“Ė½ā“šøĆĢā£®
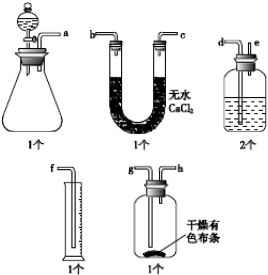
½ā“š ½ā£ŗ£Ø1£©ŹµŃé×°ÖƵÄĮ¬½ÓĖ³Šņ£¬×ńŃ”°·¢Éś×°ÖĆ-³żŌÓ×°ÖĆ-ŠŌÖŹ¼ģŃé×°ÖĆ-ĘųĢåŹÕ¼Æ×°ÖĆ-Ī²Ęų“¦Ąķ×°ÖĆ”±£¬¹ŹĘäĮ¬½ÓĖ³ŠņĪŖ£ŗa½Ó£Ød£©”¢£Øe£©½Ó£Øb»ņc£©”¢£Øc»ņb£©½Ó£Øg£©”¢£Øh£©½Ó£Øe£©”¢£Ød£©½Ó£Øf£©£¬
¹Ź“š°øĪŖ£ŗd£»e£»b£»c£»g£»h£»e£»d£»f£»
£Ø2£©ĀČĘųŅ²æÉÓĆÅØĮņĖįøÉŌļ£¬ÓĆĻ“ĘųĘæĢę“śUŠĪ¹Ü£¬¹Ź“š°øĪŖ£ŗÅØĮņĖį£»
£Ø3£©¶ŌÓŚÓŠĘųĢåÉś³ÉµÄ×°ÖĆ£¬ŹµŃé½ųŠŠĒ°¶¼Ó¦¶Ō×°ÖƵÄĘųĆÜŠŌ½ųŠŠ¼ģ²é£¬¹Ź“š°øĪŖ£ŗ¼ģ²é×°ÖƵÄĘųĆÜŠŌ£»
£Ø4£©øÉŌļµÄĀČĘų²»¾ßÓŠĘư׊Ō£¬¹Ź“š°øĪŖ£ŗ·ń£»
£Ø5£©¶ŌÓŚĘųĢåµÄŹÕ¼Æ£¬Čō·“Ó¦ŗóĪŽ·ØŹÕ¼Æµ½ĘųĢ壬æÉ“Ó×°ÖƵÄĘųĆÜŠŌ”¢·“Ó¦µÄ·¢Éś½ųŠŠæ¼ĀĒ£¬ČēĖįµÄÅØ¶ČŠ”£¬×°ÖĆĀ©Ęų£¬»ņ×°ÖĆĮ¬½Ó“ķĪó£¬
¹Ź“š°øĪŖ£ŗŃĪĖįÅØ¶ČŠ”£¬·“Ӧƻ·¢Éś£» ×°ÖĆĀ©Ęų£» eÓėfĮ¬½Ó£®
µćĘĄ ±¾Ģāæ¼²éĮĖĀČĘųµÄÖʱøŗĶŠŌÖŹŹµŃ飬ĪŖøßĘµæ¼µć£¬½įŗĻĮĖŹµŃé×°ÖĆ×ŪŗĻæ¼²éĮĖŹµŃéµÄĮ¬½ÓŅŌ¼°ŹµŃé×°ÖƵÄ×÷ÓĆ£¬ŹĒŅ»µĄ·Ē³£ÓŠ¼ŪÖµµÄĢāÄ森¼Čæ¼²éĮĖѧɜµÄ»ł“”ÖŖŹ¶£¬ÓÖ×ŪŗĻæ¼²éĮĖѧɜµÄ¶ÆŹÖŹµŃéÄÜĮ¦£®


 ĶõŗóŠŪѧ°ø½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
ĶõŗóŠŪѧ°ø½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø ŗ£µķæĪŹ±ŠĀ×÷Ņµ½š°ń¾ķĻµĮŠ“š°ø
ŗ£µķæĪŹ±ŠĀ×÷Ņµ½š°ń¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé | ĻÖĻó | ½įĀŪ |
| A | ÓĆ²£Į§°ōÕŗČ”“ĪĀČĖįÄĘČÜŅŗ£¬µćŌŚpHŹŌÖ½ÉĻ | ŹŌÖ½×īÖÕĻŌĄ¶É« | “ĪĀČĖįÄĘČÜŅŗĻŌ¼īŠŌ |
| B | ½«Ķ·Ū¼ÓČė1.0mol/L Fe2£ØSO4£©3ČÜŅŗÖŠ | ČÜŅŗ±äĄ¶”¢ÓŠŗŚÉ«¹ĢĢå³öĻÖ | ½šŹōĢś±ČĶ»īĘĆ |
| C | ÓĆŪįŪöĒƼŠ×”Ņ»Š”æéÓĆɰֽ׊Ļø“ņÄ„¹żµÄĀĮ²ŌŚ¾Ę¾«µĘÉĻ¼ÓČČ | ČŪ»ÆŗóµÄŅŗĢ¬ĀĮµĪĀäĻĀĄ“ | ½šŹōĀĮµÄČŪµć½ĻµĶ |
| D | ½«0.1mol/L MgSO4ČÜŅŗµĪČėNaOHČÜŅŗÖŠÖĮ²»ŌŁÓŠ³Įµķ²śÉś£¬ŌŁµĪ¼Ó0.1mol/L CuSO4ČÜŅŗ | °×É«³Įµķ±äĪŖĄ¶É«³Įµķ | Cu£ØOH£©2µÄČܽā¶Č±ČMg£ØOH£©2µÄŠ” |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
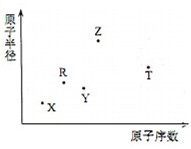 ¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢Z”¢R”¢TµÄŌ×Ó°ė¾¶ÓėŌ×ÓŠņŹż¹ŲĻµČēĶ¼ĖłŹ¾£®RŌ×Ó×īĶā²ćµē×ÓŹżŹĒµē×Ó²ćŹżµÄ2±¶£®YÓėZÄÜŠĪ³ÉZ2Y”¢Z2Y2ŠĶĄė×Ó»ÆŗĻĪļ£®ZÓėTŠĪ³ÉµÄ»ÆŗĻĪļZ2T£®ĻĀĮŠĶʶĻ“ķĪóµÄŹĒ£Ø””””£©
¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢Z”¢R”¢TµÄŌ×Ó°ė¾¶ÓėŌ×ÓŠņŹż¹ŲĻµČēĶ¼ĖłŹ¾£®RŌ×Ó×īĶā²ćµē×ÓŹżŹĒµē×Ó²ćŹżµÄ2±¶£®YÓėZÄÜŠĪ³ÉZ2Y”¢Z2Y2ŠĶĄė×Ó»ÆŗĻĪļ£®ZÓėTŠĪ³ÉµÄ»ÆŗĻĪļZ2T£®ĻĀĮŠĶʶĻ“ķĪóµÄŹĒ£Ø””””£©| A£® | ŠĪ³ÉµÄ¼ņµ„Ąė×Ó°ė¾¶µÄ“óŠ”Ė³ŠņĪŖT£¾Y£¾Z | |
| B£® | Z2Y”¢Z2Y2Ėłŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶĻąĶ¬ | |
| C£® | 0.005mol•L-1TµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖ®ČÜŅŗpHµČÓŚ2 | |
| D£® | Z2TµÄĖ®ČÜŅŗĻŌ¼īŠŌ£¬¶ŌĖ®µÄµēĄėÓŠ“Ł½ų×÷ÓĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 +
+ ”ś
”ś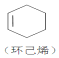
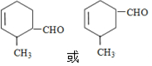 £®
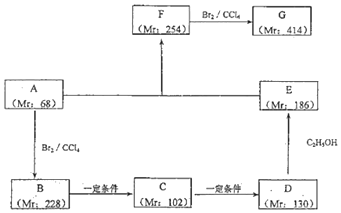
£®
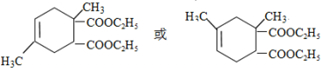 £®
£®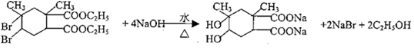 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
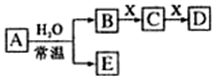 A”¢B”¢C”¢D”¢E”¢X¾łĪŖ֊ѧ»Æѧ³£¼ūĪļÖŹ£¬ĘäÖŠA”¢B”¢C”¢D”¢EŹĒÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄĪŽ»śĪļ£¬ĖüĆĒ“ęŌŚČēĶ¼×Ŗ»Æ¹ŲĻµ£Ø²æ·ÖÉś³ÉĪļŗĶ·“Ó¦Ģõ¼žĀŌČ„£©£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
A”¢B”¢C”¢D”¢E”¢X¾łĪŖ֊ѧ»Æѧ³£¼ūĪļÖŹ£¬ĘäÖŠA”¢B”¢C”¢D”¢EŹĒÓɶĢÖÜĘŚŌŖĖŲ×é³ÉµÄĪŽ»śĪļ£¬ĖüĆĒ“ęŌŚČēĶ¼×Ŗ»Æ¹ŲĻµ£Ø²æ·ÖÉś³ÉĪļŗĶ·“Ó¦Ģõ¼žĀŌČ„£©£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ £» BÓėX·“Ӧɜ³ÉCµÄĄė×Ó·½³ĢŹ½2OH-+CO2=CO32-+H2O£»
£» BÓėX·“Ӧɜ³ÉCµÄĄė×Ó·½³ĢŹ½2OH-+CO2=CO32-+H2O£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
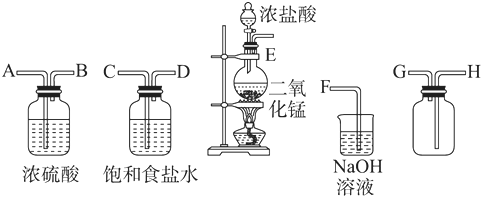
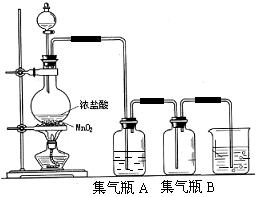 ŹµŃéŹŅÖŠĖłÓĆÉŁĮæĀČĘųŹĒÓĆĻĀĮŠ·½·ØÖĘČ”µÄ£¬4HCl£ØÅØ£©+MnO2$\frac{\underline{\;\;”÷\;\;}}{\;}$Cl2”ü+MnCl2+2H2O
ŹµŃéŹŅÖŠĖłÓĆÉŁĮæĀČĘųŹĒÓĆĻĀĮŠ·½·ØÖĘČ”µÄ£¬4HCl£ØÅØ£©+MnO2$\frac{\underline{\;\;”÷\;\;}}{\;}$Cl2”ü+MnCl2+2H2O²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
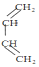
| A£® | 2øö¼×»ł£¬ÄÜÉś³É4ÖÖ-ĀČ“śĪļ | B£® | 3øö¼×»ł£¬ÄÜÉś³É5ÖÖ-ĀČ“śĪļ | ||
| C£® | 3øö¼×»ł£¬ÄÜÉś³É9ÖÖ-ĀČ“śĪļ | D£® | 4øö¼×»ł£¬ÄÜÉś³É4ÖÖ-ĀČ“śĪļ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com