
| 盐酸 | (NH4)2SO4溶液 | |
| 由水电离出的氢离子浓度 | 1.0×10-amol•L-1 | 1.0×10-b mol•L-1 |
| A. | 盐酸中水的离子积大于(NH4)2SO4溶液中水的离子积 | |
| B. | 盐酸和硫酸铵溶液均抑制了水的电离 | |
| C. | 盐酸的pH=a | |
| D. | 在(NH4)2SO4溶液中:c(NH4+)+c(NH3•H2O)=2c(SO42-) |
分析 A.均为常温下,Kw与温度有关;
B.硫酸铵为强酸弱碱盐,可发生水解反应;
C.盐酸中由水电离出的氢离子浓度为1.0×10-amol•L-1,可知1.0×10-amol•L-1×c(H+)酸=1×10-14;
D.(NH4)2SO4溶液,n(N)=2n(S),结合物料守恒判断.
解答 解:A.温度相同,则酸中水的离子积等于(NH4)2SO4溶液中水的离子积,故A错误;
B.盐酸抑制水的电离,硫酸铵促进水的电离,故B错误;
C.盐酸中由水电离出的氢离子浓度为1.0×10-amol•L-1,可知1.0×10-amol•L-1×c(H+)酸=1×10-14,则盐酸的pH为14-a,故C错误;
D.(NH4)2SO4溶液,n(N)=2n(S),由物料守恒可知c(NH4+)+c(NH3•H2O)=2c(SO42-),故D正确;
故选D.
点评 本题考查离子浓度关系及盐类水解,为高频考点,把握Kw与温度的关系、pH的计算、物料守恒为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “真金不怕火炼”说明有些金属(例如金)即使在高温下也不与氧气发生反应 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 含重金属离子的电镀废液不能随意排放 | |
| D. | 铜的金属活泼性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质在一定条件下均能水解 | |
| B. | 乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物 | |
| C. | 分子式为C4H8C12的有机物共有(不含立体异构)8种 | |
| D. | 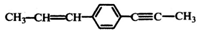 处于同一平面上的原子数最多为18个 处于同一平面上的原子数最多为18个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
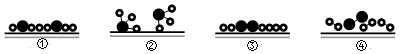
| A. | ④③①② | B. | ③④①② | C. | ③④②① | D. | ④③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作设计 | 现象记录 | 结论解释 | |
| A | 醋酸加入到碳酸钠固体中,将产生的气体通入C6H5ONa 溶液中 | 溶液变浑浊 | 酸性:CH3COOH>H2CO3>C6H5OH |
| B | CH3CH2Br 与NaOH 乙醇溶液共热产生的气体通入溴水中 | 溶液褪色 | 产生了乙烯 |
| C | 向某氯化亚铁溶液中加入加入Na2O2 粉末 | 出现红褐色沉淀 | 加入 Na2O2 粉末前,原氯化亚铁溶液已经变质 |
| D | 向紫色石蕊试液中持续长时 间通人氯气 | 溶液先变红,最后变为无色 | 氯气有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在在氯气中燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | CaCO3与稀盐酸反应制取CO2 | D. | CaO溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
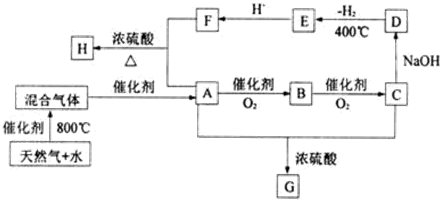
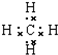 ;E的化学式是Na2C2O4.
;E的化学式是Na2C2O4.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com