
| A. | A、B、E一定处于三个不同的短周期 | |
| B. | A、D不可能在同一主族 | |
| C. | C的最高价氧化物对应的水化物可能显碱性 | |
| D. | C和D的单质不可能化合成1:1型离子化合物 |
分析 A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,B、E是同主族元素,由原子序数可知,B处于第二周期、E处于第三周期,由于原子半径A<B,核电荷数A<B,因为同周期,原子序数越小,半径越大,因而A、B也不在同一周期中,则A应在第一周期,故A为氢元素;原子半径D>E,核电荷数D<E,根据同周期原子半径的递变规律可知,D、E处于相同周期,则D应处于第三周期;原子半径B>C,核电荷数B<C,根据同周期原子半径的递变规律可知,B、C在相同周期,以此解答该题.
解答 解:A.由上述分析可知,A在第一周期,B在第二周期,E在第三周期,故A正确;
B.A为氢元素,若D为第三周期的Na时,则A、D在同一主族,故B错误;
C.E处于第三周期,B、C处于第二周期,由于原子半径E>B>C,则B不可能为Li,则C一定为非金属,其最高价氧化物对应的水化物显酸性,故C错误;
D.由于C为非金属,D为可能为金属Na等,则C、D的单质有可能形成1:1型离子化合物,如Na2O2,故D错误;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数与原子半径的大小、元素周期律中的递变规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 40% | B. | 50% | C. | 80% | D. | 90% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HCl>HI | B. | 结合质子能力:S2->Cl- | ||
| C. | 原子半径:Ge>As | D. | 酸性:HNO2>HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | N≡N | N-H | H-H |
| 键能(kJ/mol) | 942 | 391 | b |
| A. | 551 | B. | 437 | C. | 558 | D. | 160 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
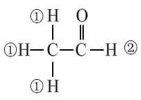 已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在核磁共振氢谱(1HNMR)中会给出相同的峰(信号),峰的强度与H原子数成正比.例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l.
已知化合物分子结构中的等效氢原子(在化合物的结构中所处的环境相同的H原子)在核磁共振氢谱(1HNMR)中会给出相同的峰(信号),峰的强度与H原子数成正比.例如:乙醛的结构中有①②两类氢原子且个数比为3:1,它在1HNMR谱中也有2个信号峰,其强度之比为3:l.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯和乙酸均能与氢气发生加成反应 | |
| B. | 某芳香烃的分子式为C10H14,常温下它可使酸性KMnO4溶液褪色,且分子结构中只有一个侧链,符合条件的烃有4种 | |
| C. | 1 mol的有机物(结构如图 )最多能与含5mol NaOH的水溶液完全反应 )最多能与含5mol NaOH的水溶液完全反应 | |
| D. | 蛋白质盐析会使蛋白质失去生理活性,加热、紫外线照射等措施可使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④⑥ | C. | ③④⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 温度/℃ | 物质的起始浓度/mol•L-1 | 物质的平衡浓度/mol•L-1 | ||
| c(X) | c(Y) | c(Z) | c(Z) | ||
| I | 758 | 0.2 | 0.1 | 0 | 0.1 |
| Ⅱ | 758 | 0.1 | 0.05 | 0 | |
| Ⅲ | 858 | 0.2 | 0.1 | 0 | |
| A. | 从开始至平衡时,容器I中Z的反应速率为0.044 mol•L-1•s-1 | |
| B. | 平衡时,容器Ⅱ中Z的浓度为0.05 mol•L-1 | |
| C. | 平衡时,容器Ⅲ中Z的浓度大于0.1 mol•L-1 | |
| D. | 若起始时向容器I中充入0.02 mol X、0.01 mol Y和0.02 mol Z,则反应向正反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
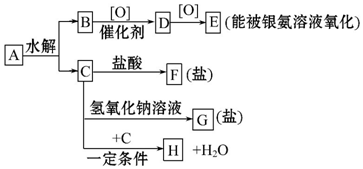
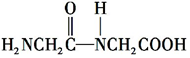 +H2O.
+H2O.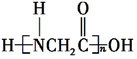 +(n-1)H2O.
+(n-1)H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com