
| A. | (NH4)2 SO4 | B. | Al(OH)3 | C. | NaHSO4 | D. | Mg(NO3)2 |
科目:高中化学 来源: 题型:解答题
 )可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
)可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
 (X代表卤素原子);
(X代表卤素原子);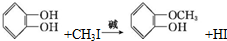 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S有强还原性(1)用于除去废水中的Cu2+ 和Hg2+(2) | |
| B. | CaCO3是难容物(1)CaCO2溶液中通入CO2产生白色沉淀(2) | |
| C. | 浓HSO4有强氧化性(1),浓H2SO4可用于干燥SO2(2) | |
| D. | Zn具有还原性和导电性(1)可用锌锰干电池的负极材料(2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A一定不是气态物质 | B. | A一定是气态物质 | ||
| C. | B一定不是气态物质 | D. | B一定是气态物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做一次完整的中和热的测定实验,至少需要使用温度计测4次数据 | |
| B. | 向酸性重铬酸钾溶液中少量加NaOH固体,溶液颜色由橙色慢慢变为黄色 | |
| C. | 分别向两支盛有浓度相等的醋酸和饱和硼酸溶液中滴加等浓度的Na2CO3溶液,观察到前者产生气泡不如后者剧烈 | |
| D. | 在0.01mol/L的KMnO4溶液中加入0.1mol/L的H2C2O4溶液,实验开始时溶液褪色很快,后来逐渐变慢,主要是由于溶液浓度变化所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离饱和食盐水与沙子的混合物 | |
| B. | 分离水和汽油的混合物 | |
| C. | 分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物. | |
| D. | 从硝酸钾和氯化钠的混合液中获得硝酸钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用100mL容量瓶配制50mL 0.1mol/L的盐酸 | |
| B. | 用10mL 量筒量取5.2mL盐酸 | |
| C. | 用托盘天平称取25.12g NaCl固体 | |
| D. | 用pH试纸测得某溶液的pH值为12.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com