
| A. | 28 g铁粉与酸反应失去的电子数是NA | |
| B. | 标准状况下,11.2 L NH3含有的原子总数为1.5NA | |
| C. | 0.5 mol•L-1 K2SO4溶液中所含K+的数目为NA | |
| D. | 46 g N02和N2O4的混合气体含有的原子总数为3NA |
分析 A.铁与氧化性酸反应生成三价铁离子,与非氧化性酸反应生成二价铁离子;
B.氨气为四原子分子;
C.溶液体积未知;
D.NO2和N2O4最简式相同为NO2,计算46gNO2中所含原子数.
解答 解:A.铁与酸反应转移电子数,与酸的类型与酸的用量有关,例如与足量硝酸反应生成硝酸铁,与少量硝酸反应生成硝酸亚铁,盐酸与铁反应生成氯化亚铁,所以酸的类型、用量不确定,无法计算转移电子数,故A错误;
B.标准状况下,11.2 L NH3含有的原子总数为$\frac{11.2L}{22.4L/mol}$×4×NA=2NA,故B错误;
C.依据n=CV,溶液体积未知,无法计算硫酸钾的物质的量,无法计算钾离子个数,故C错误;
D.NO2和N2O4最简式相同为NO2,计算46gNO2中所含原子数$\frac{46g}{46g/mol}$×3×NA=3NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的分析应用,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确气体摩尔体积的条件应用是解题关键,题目难度不大.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:解答题
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:W>X>Y | |
| B. | W的简单气态氢化物的热稳定性比Y的弱 | |
| C. | Z分别与Q、X形成的化合物中化学键类型相同 | |
| D. | X的最高价氧化物对应水化物的碱性在同周期中最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
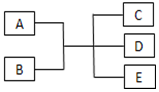 已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如图反应关系.
已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如图反应关系.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 泡沫灭火器的反应原理是非氧化还原反应 | |
| B. | 钢铁析氢腐蚀和吸氧腐蚀的速率一样快 | |
| C. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| D. | 燃料电池的燃料都在负极发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14 g乙烯气体中的氢原子数约为2×6.02×1023 | |
| B. | 标准状况下,2.24 L H2O含有的共价键数约为0.2×6.02×1023 | |
| C. | 1 mol N2与3 mol H2反应生成的NH3分子数约为2×6.02×1023 | |
| D. | 0.1 L 0.5 mol/L CH3COOH溶液中含有的氢离子数约为0.05×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+为重金属离子,故CuSO4不能用于生活用水消毒 | |
| B. | 卤水煮豆腐是Mg2+、Ca2+等使蛋白质胶体发生凝聚过程 | |
| C. | 纯碱溶液可以洗涤餐具上的油渍 | |
| D. | 油漆刷在钢铁护栏表层用来防止金属锈蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com