
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示。下列描述正确的是( )

A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B. 反应的化学方程式为X(g)+Y(g)![]() Z(g)
Z(g)
C. 每消耗1molX同时生成2mol Z,说明反应已达平衡
D. 反应开始到10s时,Y的转化率为79.0%
【答案】D
【解析】
A. 反应开始到10s生成Z是1.58mol,浓度是1.58mol÷2L=0.79mol/L,则用Z表示的反应速率为0.79mol/L÷10s=0.079mol/(L·s),A错误;
B. 根据图像可知X与Y是生成物,Z是反应物,平衡时消耗X是1.2mol-0.41mol=0.79mol,消耗Y是1.00mol-0.21mol=0.79mol,生成Z是1.58mol,根据变化量之比是化学计量数之比可知反应的化学方程式为X(g)+Y(g)![]() 2Z(g),B错误;
2Z(g),B错误;
C. 每消耗1molX同时生成2mol Z均表示正反应速率,不能说明反应已达平衡,C错误;
D. 反应开始到10s时,Y的转化率为0.79mol/1.00mol×100%=79.0%,D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】Kolbe法制取乙烯的装置如图所示,电极a上的产物为乙烯和碳酸根离子。下列说法正确的是( )

A. 该装置将化学能转化为电能
B. 图中为阳离子交换膜
C. 阴极周围溶液的pH不断减小
D. 每生成1mol乙烯,电路中转移2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下表提供数据及相关物质结构知识,反应1:SiCl4(g)+2H2(g)=Si(g)+4HCl(g),反应2:Si(g)+O2(g)=SiO2(g),则反应1和反应2的反应热为
 硅的晶体结构
硅的晶体结构
化学键 | Si-Cl | H-H | Si-Si | H-Cl | O=O | Si-O |
键能kJ/mol) | 360 | 436 | 176 | 431 | 498 | 460 |
A. +236kJ/mol,-990kJ/mol B. -116kJ/mol,-990kJ/mol
C. -116kJ/mol,-70kJ/mol D. +236kJ/mol,-70kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,下列叙述不正确的是( )
A.用活性炭可去除冰箱中的异味
B.单质硅是将太阳能转变为电能的常用材料
C.医用酒精的浓度通常为95%
D.硅胶可用作食品干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)![]() 。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示。当升高温度,再次达到平衡时,v正 v逆可能落在A、B、C、D、E哪些点。
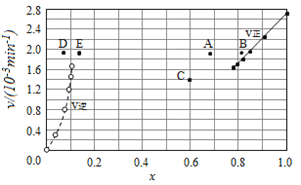
A. A D B. B D C. B E D. A E
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】收集NO和NO2两种气体( )
A. 都可用排水法 B. NO用排水法,NO2用向上排气法
C. 都可用向上排气法 D. NO用向上排气法,NO2用排水法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的电子式______________,A的结构简式_______________;
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式___________,反应类型______________;
(3)在碘水中加入B振荡静置后的现象 __________________________________;
(4)B与Br2在FeBr3催化下反应的化学反应方程式_________________________,反应类型___________。
(5)等质量的A、B完全燃烧时消耗O2的物质的量____________(填“A>B”或“A<B”或“A=B”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一份含有FeCl3和FeCl2的固体混合物,为测定各成分的含量进行如下两个实验:
实验1:①称取一定质量的样品,将样品溶解;
②向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;
③将沉淀过滤、洗涤、干燥得到白色固体17.22 g。
实验2:①称取与实验1中相同质量的样品,将样品溶解;
②向溶解后的溶液中,通入足量的Cl2;
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀;
④将沉淀过滤、洗涤后,加热灼烧至质量不再减少,得到固体物质4 g。
根据实验回答下列问题:
(1)溶解过程中所用到的玻璃仪器有________________________。
(2)实验室配制FeCl2溶液时通常会向其中加入少量试剂________________。
(3)“实验2”通入足量Cl2的目的是_________。涉及的化学反应的离子方程式是__________。
(4)检验“实验2”的步骤④中沉淀已经洗涤干净的方法是________________。
(5)加热FeCl3溶液,并将溶液蒸干时,通常不能得到FeCl3固体,请以平衡的观点解释其原因(化学方程式与文字相结合来说明)____________________________________。
(6)FeCl3溶液可以用于止血,主要是因为FeCl3溶液能使血液聚沉,这涉及胶体的相关性质。以下关于胶体的说法正确的是________
A.胶体的分散质能透过滤纸
B.实验室制备胶体Fe(OH)3胶体,是将饱和FeCl3溶液滴入热的NaOH溶液中,加热至溶液变为红褐色
C.当光束通过胶体时能产生丁达尔效应
D.胶体、溶液、浊液中,含分散质粒子直径最大的分散系是胶体
(7)通过实验所得数据,计算固体样品中FeCl3和FeCl2的物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学反应方程式,并判断其反应类型(加成、取代、氧化)
①甲烷与氯气反应_______________________________,属于________反应
②乙烯通入溴水:_________________________________,属于________反应
③乙醇与金属钠反应:__________________________________,属于________反应
④由苯制取硝基苯:_______________________________,属于________反应;
⑤灼热的铜丝多次反复地插入乙醇中:___________________,属于_______反应;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com