
���� ���ݵ���غ��������������c��H+��=c��OH-��=10-7mol/L��c��Na+��=c��CH3COO-��=0.005mol/L���μ�NaOHˮ�ĵ��������ƣ�����ƽ�������ƶ����Դ˼��㣮
��� �⣺�ɵ���غ��֪��c��Na+��+c��H+��=c��OH-��+c��CH3COO-������֪��Һ��c��CH3COO-���Tc��Na+������c��H+��=c��OH-��������Һ�����ԣ���������c��H+��=c��OH-��=10-7mol/L��c��Na+��=c��CH3COO-��=0.005mol/L�������ú�b�Ĵ���ʽ��ʾCH3COOH�ĵ��볣��Ka=$\frac{1{0}^{-7}��0.005}{\frac{b}{2}-0.005}$=$\frac{1{0}^{-9}}{b-0.01}$���μ�NaOHˮ�ĵ��������ƣ�����ƽ�������ƶ���
�ʴ�Ϊ���У�$\frac{1{0}^{-9}}{b-0.01}$������
���� ���⿼��������ϵļ���Ͷ��Է���������ѧ���������������������Ŀ��飬�漰����ϡ�pH��Ũ�ȵĹ�ϵ�ȣ�ע�����غ�������غ��Ӧ�ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
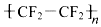 ���IJ��ϣ�
���IJ��ϣ�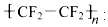 �Dz�ճ��Ϳ�����ʵ���Ҫ�ɷ֣������й�˵������ȷ���ǣ�������
�Dz�ճ��Ϳ�����ʵ���Ҫ�ɷ֣������й�˵������ȷ���ǣ�������| A�� | CF2=CF2��ʹ���CCl4��Һ��ɫ | |
| B�� | �ķ���ϩ�ϳɾ��ķ���ϩ���ڼӾ۷�Ӧ | |
| C�� | 1molCF2=CF2ֻ����1molH2�����ӳɷ�Ӧ | |
| D�� | 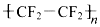 ��ʹ�������������Һ��ɫ ��ʹ�������������Һ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10 | B�� | 50 | C�� | 5��l03 | D�� | 104 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��x��nʱ����Ӧ�����ӷ���ʽΪ��2Fe2++Cl2�T2Fe3++2Cl- | |
| B�� | ��x��$\frac{3n}{2}$ʱ����Ӧ�����ӷ���ʽΪ��2Fe2++2I-+2Cl2�T2Fe3++I2+4Cl- | |
| C�� | ��n��x��$\frac{3n}{2}$ʱ����Ӧ��ת�Ƶ��ӵ����ʵ���n��e-��Ϊ2nmol��n��e-����3nmol | |
| D�� | ��n��x��$\frac{3n}{2}$ʱ����Һ��Fe3+��Cl-��I2�����ʵ���֮��Ϊ2��x-n����x��n |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ķ��������Է���е����ϴ�Ĺ������� | |
| B�� | ���Ļ�����Ӧ��ʮ�ֹ㷺����FeCl3��FeSO4�������ľ�ˮ�� | |
| C�� | þȼ�շ���ҫ�۵İ⣬�����������źŵ������ | |
| D�� | ��ҵ����������ʯ����Ϊԭ������Ư�ۣ�Ư����Ҫ�ɷ�ΪCa��ClO��2��CaCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ�͵ķ�����ѻ������ڻ�ѧ�仯 | |
| B�� | �����͡�ʯ�͡����ͺ�ţ�;����ڸ�֬��������� | |
| C�� | ú�ڿ����о�������ǿ���Ƶý�̿�����Ȼ���ԭ�� | |
| D�� | ���͡�����ͨ����Ϊ������ȼ�ϣ���һ������ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | z=4 | B�� | B��ת������40% | ||
| C�� | A��ƽ��Ũ����1.4 mol•L-1 | D�� | ƽ��ʱ����ѹǿ��ԭ����1.2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��CH3COO-����c��Ba2+����c��OH-����c��H+�� | B�� | c��H+��+c��Ba2+��=c��CH3COO-��+c��OH-�� | ||
| C�� | c��OH-���Tc��H+��+c��CH3COO-�� | D�� | 2c��Ba2+��=c��CH3COO-��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״����.22.4LH2S��SO2�Ļ�������к��еķ�������ΪNA | |
| B�� | 1L1mol•L-1FeCl3��Һ��ȫˮ�������Fe��OH��3����������ΪNA | |
| C�� | ������.16.8gFe��������ˮ������ȫ��Ӧʧȥ�ĵ�����Ϊ0.8NA | |
| D�� | 28.6gNa2CO3•10H2O����ˮ���1L��Һ������Һ����������ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com